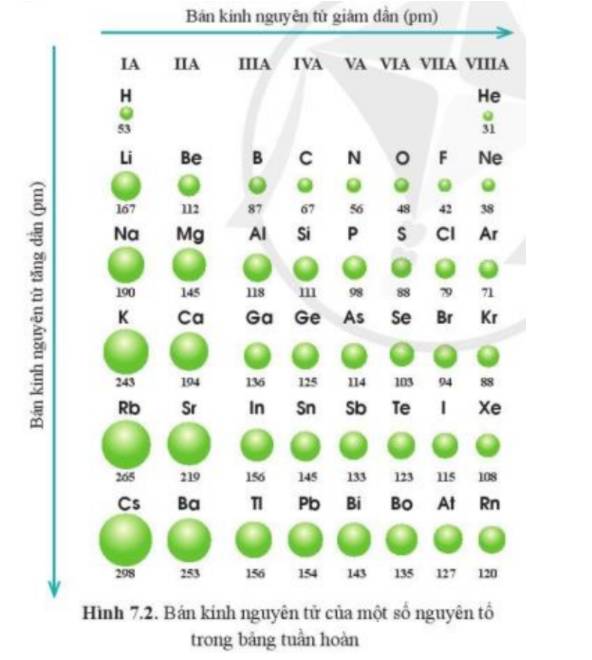
Quan sát hình 7.2, cho biết quy luật biến đổi bán kính nguyên tử của các nguyên tố ở chu kì 3, 4, 5 theo chiều tăng dần điện tích hạt nhân.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
(3) Tính kim loại, tính phi kim của các nguyên tố biến đổi tuần hoàn theo chiều tăng dần của điện tích hạt nhân
(5) Proton và notron là các thành phần cấu tạo của hạt nhân nguyên tử

Chọn đáp án B
(1) Đúng. Điện tích tăng dần → sức hút giữa lớp vỏ và hạt nhân tăng → bán kính giảm dần.
(2) Sai. Tính kim loại tăng dần → độ âm điện giảm dần.
(3) Đúng. Liên kết giữa kim loại mạnh và phi kim mạnh luôn có hiệu độ âm điện > 1,7.
(4) Sai. Nguyên tử N trong HNO3 cộng hoá trị là 4 (là hoá trị cao nhất của nitơ)
(5) Đúng.

Chọn đáp án B
(1) Đúng. Điện tích tăng dần → sức hút giữa lớp vỏ và hạt nhân tăng → bán kính giảm dần.
(2) Sai. Tính kim loại tăng dần → độ âm điện giảm dần.
(3) Đúng. Liên kết giữa kim loại mạnh và phi kim mạnh luôn có hiệu độ âm điện > 1,7.
(4) Sai. Nguyên tử N trong HNO3 cộng hoá trị là 4 (là hoá trị cao nhất của nitơ)
(5) Đúng.
Các nguyên tố chu kì 3, 4, 5 theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử giảm dần từ trái quá phải.