Câu 6: Đốt cháy 12,4g Phosphorus trong bình chứa 18g khí Oxygen tạo thành Diphosphorus Pentoxide P2O5 .
a. Chất nào còn dư sau phản ứng ? Khối lượng chất dư là bao nhiêu ?
b. Chất nào được tạo thành ? Khói lượng là bao nhiêu ?
giúp tui với mai nộp rui ah :<

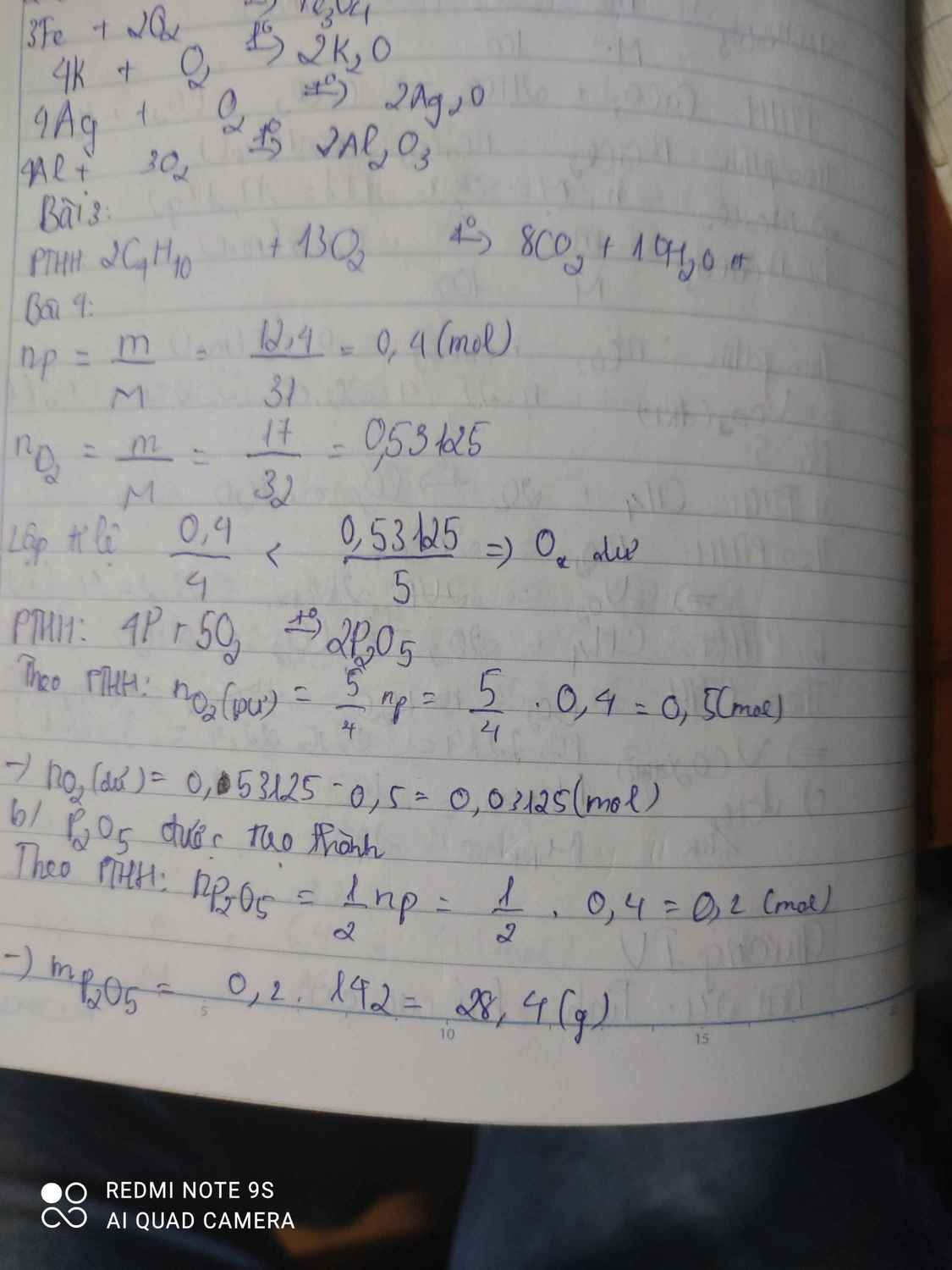
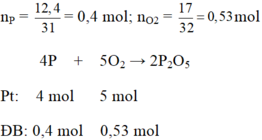

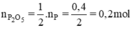

\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{18}{32}=0,5625\left(mol\right)\)
PTHH :
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,4 0,5 0,2
\(\dfrac{0,4}{4}< \dfrac{0,5625}{5}\) --> O2 dư sau phản ứng
\(m_{O_2dư}=\left(0,5625-0,5\right).32=2\left(g\right)\)
P2O5 được tạo thành.
\(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{18}{32}=0,5625\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
a, Xét tỉ lệ: \(\dfrac{0,4}{4}< \dfrac{0,5625}{5}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=0,5\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,0625\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,0625.32=2\left(g\right)\)
b, P2O5 được tạo thành.
Theo PT: \(n_{P_2O_5}=\dfrac{1}{2}n_P=0,2\left(mol\right)\)
\(\Rightarrow m_{P_2O_5}=0,2.142=28,4\left(g\right)\)