Hoà tan hoàn toàn 32,5 g một kim loại M ( hoá trị 2 ) bằng dung dịch FeSO4 loãng được 28gam sắt . Kim loại M là : A. Zn B. Al C.Mg D.Ca
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(n_{H_2}=\dfrac{19,04}{22,4}=0,85\left(mol\right)\)
=> mH2 = 0,85.2 = 1,7 (g)
PTHH:
A + 2HCl ---> ACl2 + H2
2B + 6HCl ---> 2BCl3 + 3H2
Theo pthh: nHCl = 2nH2 = 2.0,85 = 1,7 (mol)
-> mHCl = 1,7.36,5 = 62,05 (g)
ĐTBTKL:
mkl (A. B) + mHCl = mmuối (ACl2, BCl3) + mH2
=> a = mkl (A, B) = 76,25 + 1,7 - 62,05 = 15,9 (g)
b, Gọi nA = a (mol)
=> nAl = 5a (mol)
Theo pthh: nH2 = nA + \(\dfrac{3}{2}n_{Al}\) = a + \(\dfrac{3}{2}.5a\) = 8,5a
=> 8,5a = 0,85
=> a = 0,1 (mol)
=> nAl = 0,1.5 = 0,5 (mol)
=> mAl = 0,5.27 = 13,5 (g)
=> mA = 15,9 - 13,5 = 2,4 (g)
=> MA = \(\dfrac{2,4}{0,1}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
c, nCuO = \(\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: CuO + H2 ---to---> Cu + H2O
LTL: 0,2 < 0,85 => H2 dư
Gọi nCuO (pư) = a (mol)
=> nCu (sinh ra) = a (mol)
Ta có: mchất rắn (sau pư) = 80(0,2 - a) + 64a = 13,6
=> a = 0,15 (mol)
=> H = \(\dfrac{0,15}{0,2}=75\%\)

\(n_{H_2SO_4}=1\cdot0,2=0,2\left(mol\right)\\ PTHH:MO+H_2SO_4\rightarrow MSO_4+H_2O\\ \Rightarrow n_{MO}=n_{H_2SO_4}=0,2\left(mol\right)\\ \Rightarrow M_{MO}=\dfrac{16}{0,2}=80\left(g/mol\right)\\ \Rightarrow PTK_M=80-16=64\left(đvC\right)\)
Do đó M là Cu
Vậy chọn A
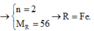
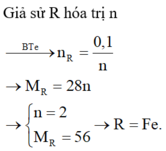
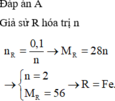
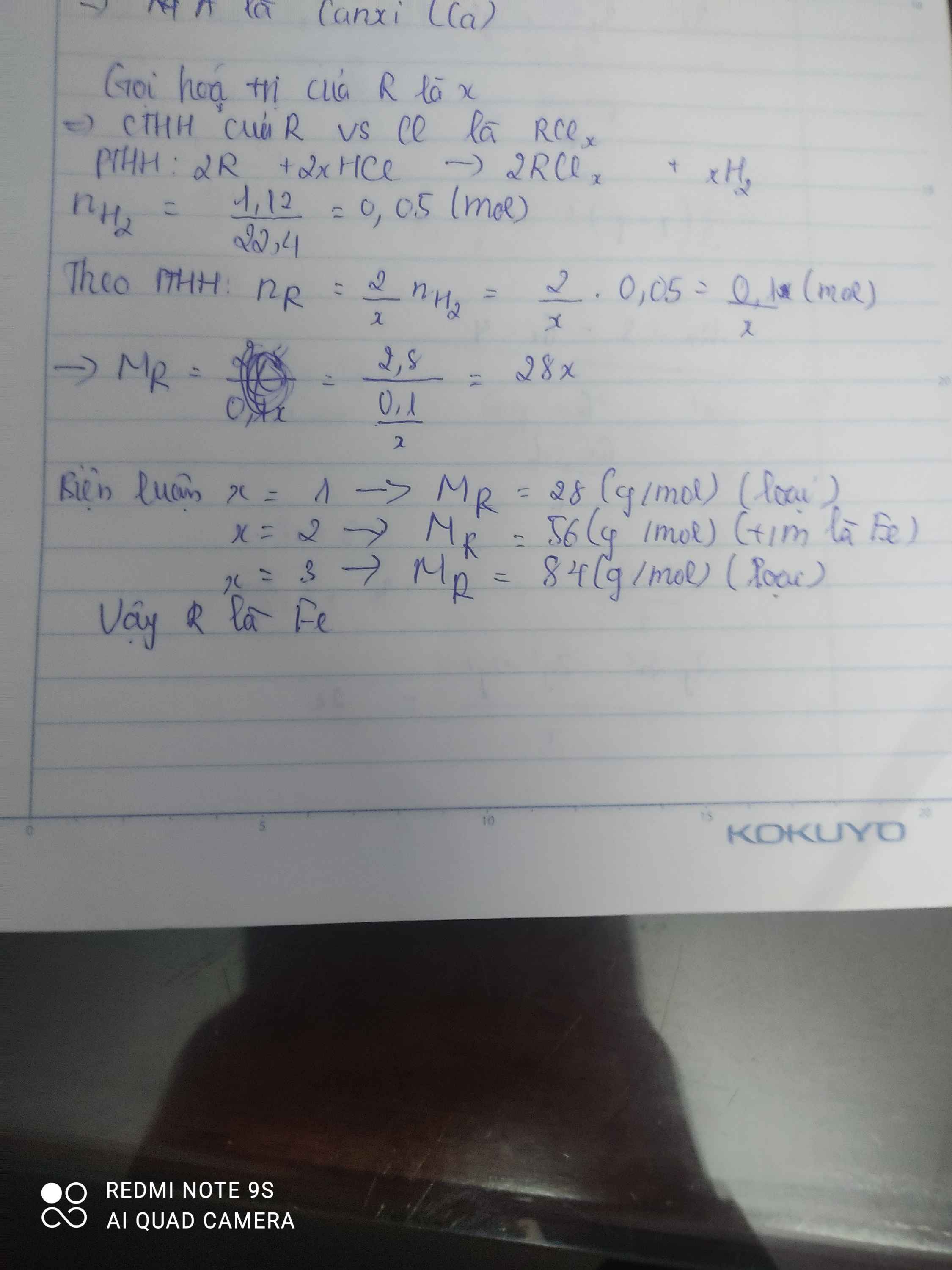

\(M+FeSO_4\rightarrow MSO_4+Fe\)
0,5 0,5
\(M_M=\dfrac{32.5}{0.5}=65\)
=>M là Zn