Lấy 200ml dung dịch H chứa đồng thời H2SO4 0,5M và HCl 2,5M rồi hòa tan vào đó 5,1gam hỗn hợp Mg,Al thấy thoát ra 5,6 lít H2(đktc).Tìm số gam mỗi kim loại trong hỗn hợp -Biết CM dd 0 đổi tìm Cm mỗi ion trong dd -Lượng muối tạo thành trong dd là ion
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a,\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: x x
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: y 1,5y
Ta có: \(\left\{{}\begin{matrix}24x+27y=12,6\\x+1,5y=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
b,\(\%m_{Mg}=\dfrac{0,3.24.100\%}{12,6}=57,14\%;\%m_{Al}=100-57,14=42,86\%\)
c,
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,3 0,3 0,3
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,2 0,3 0,1
\(C_{M_{ddH_2SO_4}}=\dfrac{0,3+0,3}{0,5}=1,2M\)
\(C_{M_{ddMgSO_4}}=\dfrac{0,3}{0,5}=0,6M;C_{M_{ddAl_2\left(SO_4\right)_3}}=\dfrac{0,1}{0,5}=0,2M\)

Gọi $n_{Mg} = n_{Al} = a(mol) ; n_{Fe} = b(mol)$
Ta có :
$24a + 27a + 56b = 15,8(1)$
$n_{HCl} > 2n_{H_2}$ nên HCl dư
Ta có :
$n_{H_2} = a + 1,5a + b = \dfrac{13,44}{22,4} = 0,6(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,1
$\%m_{Al} = \dfrac{0,2.27}{15,8}.100\% = 34,18\%$
$\%m_{Mg} = \dfrac{0,2.24}{15,8}.100\% = 30,38\%$
$\%m_{Fe} = 35,44\%$
$n_{HCl\ pư} = 2n_{H_2} = 1,2(mol)$
Bảo toàn khối lượng : $m_{muối} = 15,8 + 1,2.36,5 - 0,6.2 = 58,4(gam)$

\(n_{O_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(n_{H_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{^{t^0}}}Fe_3O_4\)
\(a.......\dfrac{2a}{3}\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
\(b.......\dfrac{3b}{4}\)
\(n_{O_2}=\dfrac{2a}{3}+\dfrac{3b}{4}=0.25\left(mol\right)\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(n_{H_2}=a+1.5b=0.45\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.15,b=0.2\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(m_{Al}=0.2\cdot27=5.4\left(g\right)\)
\(\%m_{Fe}=\dfrac{8.4}{8.4+5.4}\cdot100\%=60.8\%\)
\(\%m_{Al}=100-60.8=39.2\%\)

\(a,n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{Fe}=0,15.56=8,4(g)\\ \Rightarrow \%_{Fe}=\dfrac{8,4}{15}.100\%=56\%\\ \Rightarrow \%_{Cu}=100\%-56\%=44\%\\ b,n_{HCl}=2n_{H_2}=0,3(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,3}{0,1}=3M\)

\(a,n_{H_2}=\dfrac{2,576}{22,4}=0,115\left(mol\right)\\ Đặt:n_{Mg}=a\left(mol\right);n_{Al}=b\left(mol\right)\left(a,b>0\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \Rightarrow\left\{{}\begin{matrix}95a+133,5b=10,475\\a+1,5b=0,115\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,05\end{matrix}\right.\\ \%m_{Mg}=\dfrac{0,04.24}{0,04.24+0,05.27}.100\approx41,558\%\Rightarrow\%m_{Al}\approx58,442\%\\ b,n_{HCl}=2.n_{H_2}=2.0,115=0,23\left(mol\right)\\ \Rightarrow x=C\%_{ddHCl}=\dfrac{0,23.36,5}{100}.100=8,395\%\)
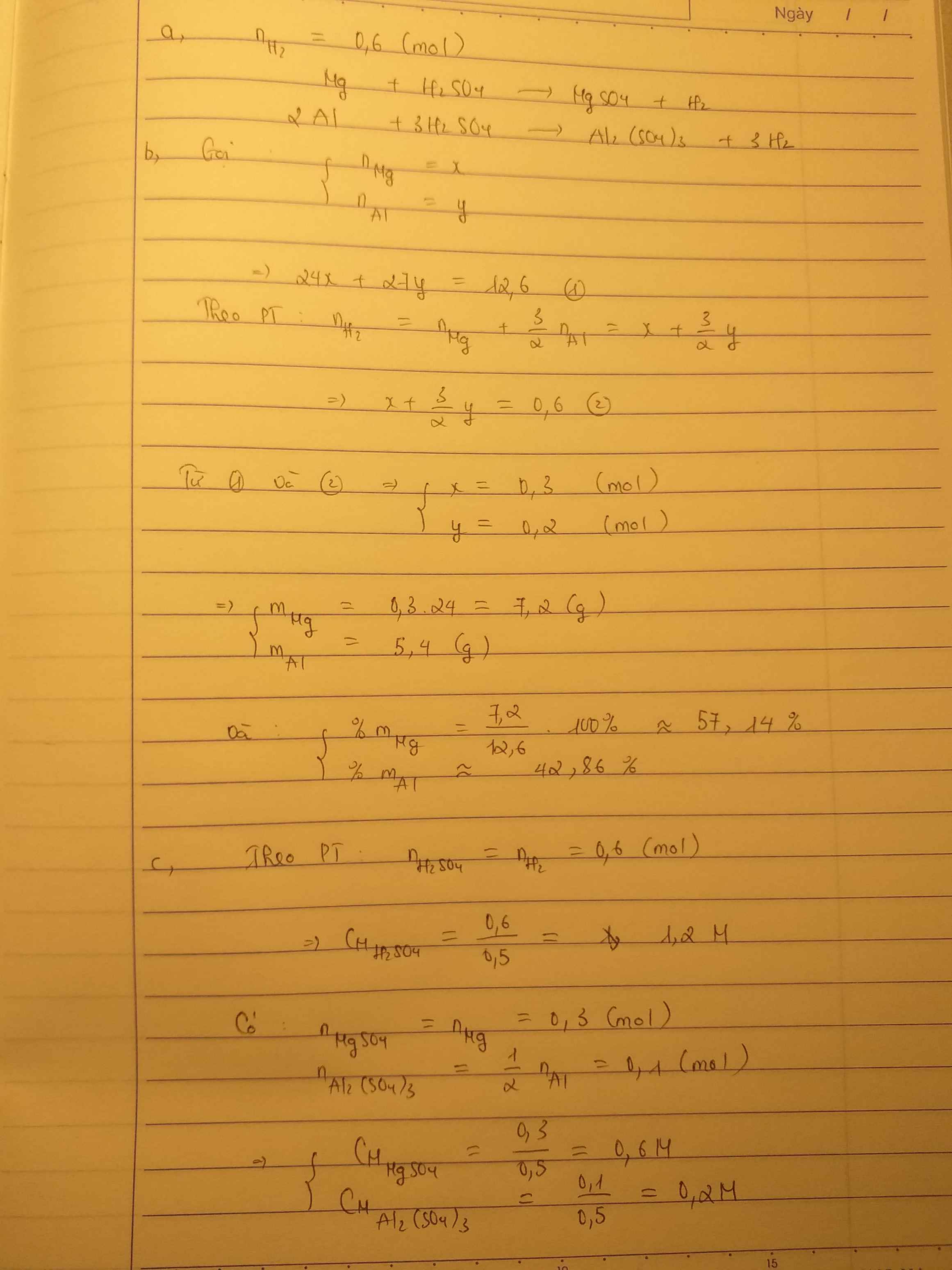

\(n_{H_2SO_4}=0,5.0,2=0,1\left(mol\right)\\ n_{HCl}=0,2.2,5=0,5\left(mol\right)\\ n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{H^+}=2n_{H_2SO_4}+n_{HCl}=0,7\left(mol\right)\)
Giả sử kim loại dư
\(\Rightarrow n_{H_2}=\dfrac{1}{2}\Sigma n_{H^+}=\dfrac{1}{2}.0,7=0,35\left(mol\right)>0,25\left(mol\right)\)
Vậy kim loại hết
Đặt \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow24x+27y=5,1\left(g\right)\) (I)
BT e:
cho:
\(Mg^o\rightarrow Mg^{2+}+2e\)
x------------------>2x
\(Al^o\rightarrow Al^{3+}+3e\)
y--------------->3y
nhận:
\(2H^++2e\rightarrow H_2O\)
0,5<--0,25
Từ trên có: \(2x+3y=0,5\left(II\right)\)
Từ (I), (II) giải được \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(CM_{H^+.dư}=\dfrac{0,7-0,5}{0,2}=1M\)
\(CM_{Mg^{2+}}=CM_{Al^{3+}}=\dfrac{0,1}{0,2}=0,5M\)
\(CM_{SO_4^{2-}}=0,5M\\ CM_{Cl^-}=2,5M\)