Có dung dịch A chứa hỗn hợp 2 muối MgCl2(10-3M) và FeCl3(10-3M)
Cho dung dịch NaOH vào dung dịch A.
a) Kết tủa nào tạo ra trước, vì sao?
b) Tìm pH thích hợp để tách một trong 2 ion Mg2+ hoặc Fe3+ ra khỏi dung dịch.
Biết rằng nếu ion có nồng độ = 10–6 M thì coi như đã được tách hết.
( Cho tích số tan của Fe(OH)3 và Mg(OH)2 lần lượt là: 10 – 39 và 10 – 11 )





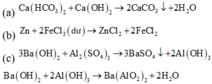

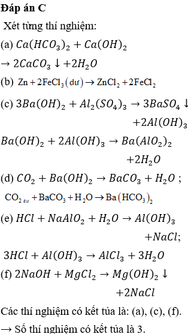

\(a.MgCl_2->Mg^{2+}+2Cl^{^{ }-};Mg^{^{ }2+}+2OH^{^{ }-}->Mg\left(OH\right)_2\\ FeCl_3->Fe^{^{ }3+}+3Cl^{^{ }-};Fe^{^{ }3+}+3OH^{^{ }-}->Fe\left(OH\right)_3\\ Tạo.Fe\left(OH\right)_3\Rightarrow\left[OH^{^{ }-}\right]\ge\sqrt[3]{\dfrac{10^{-39}}{10^{-3}}}=10^{-12}mol\cdot L^{-1}\left(1\right)\\ Tạo.Mg\left(OH\right)_2\Rightarrow\left[OH^{^{ }-}\right]\ge\sqrt{\dfrac{10^{^{ }-11}}{10^{^{ }-3}}}=10^{^{ }-4}mol\cdot L^{^{ }-1}\left(2\right)\\\left(1\right)< \left(2\right)\Rightarrow Fe\left(OH\right)_3.tạo.trước\\ b.Tạo.Mg\left(OH\right)_2:\left[OH^{^{ }-}\right]=10^{-4}\Rightarrow\left[H^+\right]=10^{-10};pH=10\\ Tạo.Fe\left(OH\right)_3:\left[Fe^{3+}\right]\le10^{-6}mol\cdot L^{-1}\Rightarrow\left[OH^-\right]^3>10^{-33}\Rightarrow\left[H^+\right]< 10^{-3}\Rightarrow pH>3\\ \Rightarrow pH:3< pH< 10 \)