cho 8.4 gam sắt tác dụng vùa đủ với dung dịch HCL kết thúc phản ứng thu được V lít khí ( đo ở đktc ) a.viết phương trình hóa học của phản ứng sảy ra b.tính giá trị của V c.đốt cháy V lít khí thu được ở trên trong 4.48 lít khí oxi (ở đktc) tính giá trị của m (biết nguyên tử khối: Na =23;H=1;CL=35.5 ;Fe=56; Zn=65; Cu=64; O=16; S=3)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe+2HCl->FeCl2+H2
0,125--0,25---0,125-0,125
m HCl=9,125 g=>n HCl=\(\dfrac{9,125}{26,5}\)=0,25 mol
=>m Fe=0,125.56=7g
=>VH2=0,125.22,4=2,8l
=>C%FeCl2=\(\dfrac{0,125.127}{7+182,5-0,25}\).100=8,388%

\(a) Fe + 2HCl \to FeCl_2\\ b) n_{HCl} = \dfrac{182,5.5\%}{36,5} = 0,25(mol)\\ n_{FeCl_2} = n_{H_2} = n_{Fe} = \dfrac{1}{2}n_{HCl} = 0,125(mol)\\ \Rightarrow m_{Fe} = 0,125.56 = 7(gam) ; V = 0,125.22,4 = 2,8(lít)\\ c) m_{dd\ sau\ phản\ ứng} = m_{Fe} + m_{dd\ HCl} - m_{H_2} = 7 + 182,5 - 0,125.2 = 189,25(gam)\\ C\%_{FeCl_2} = \dfrac{0,125.127}{189,25}.100\% = 8,39\%\)

`a)PTHH`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,125` `0,25` `0,125` `0,125` `(mol)`
`n_[HCl]=[5/100 .182,5]/[36,5]=0,25(mol)`
`b)m_[Fe]=0,125.56=7(g)`
`V_[H_2]=0,125.22,4=2,8(l)`
`c)m_[HCl]=0,25.36,5=9,125(g)`
`m_[FeCl_2]=0,125.127=15,875(g)`
`d)C%_[FeCl_2]=[15,875]/[7+182,5-0,125.2] .100~~8,39%`

\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1---->0,3
Zn + H2SO4 --> ZnSO4 + H2
0,3<--------------------0,3
=> m = 0,3.65 = 19,5 (g)

a) Mg + 2HCl \(\rightarrow\) MgCl2 + H2
Muối tạo thành: magie clorua
b) nMg = 8,4 : 24 = 0,35 mol
Theo pt: nH2 = nMg = 0,35 mol
=> V = 0,35 . 22,4 = 7,84l
c) Pt: 2Mg + O2 \(\xrightarrow[]{t^o}\) 2MgO
nO2 = 2,24 : 22,4 = 0,1 mol
Có nFe : nO2 = \(\dfrac{0,35}{2}:\dfrac{0,1}{1}=0,175:0,1\)
Do 0,175 > 0,1 nên Mg dư
nMg = 8.4 / 24 = 0.35 (mol)
Mg + 2HCl => MgCl2 + H2
0.35....................0.35....0.35
VH2 = 0.35 * 22.4 = 7.84 (g)
mMgCl2 = 0.35 * 95 = 33.25 (g)
nO2= 2.24 / 22.4 = 0.1 (mol)
2Mg + O2 -to-> 2MgO
2...........1
0.35......0.1
LTL: 0.35/2 > 0.1
=> Mg dư
Mg không cháy hết

Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít

Theo gt ta có: $n_{Al}=0,1(mol)$
a, $2Al+6HCl\rightarrow 2AlCl_3+3H_2$
b, $\Rightarrow n_{H_2}=0,15(mol)\Rightarrow V_{H_2}=3,36(l)$
c, Ta có: $n_{HCl}=0,3(mol)\Rightarrow m_{HCl}=10,95(g)\Rightarrow \%m_{ddHCl}=219(g)$
d, Bảo toàn khối lượng ta có: $m_{dd}=221,4(g)$
$\Rightarrow \%C_{AlCl_3}=6,02\%$
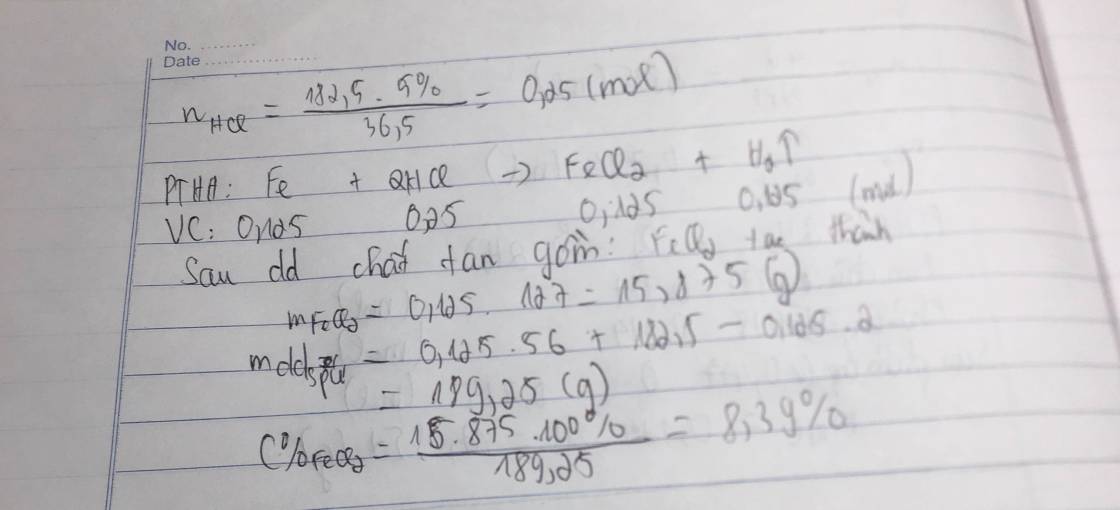


Fe+2HCl->Fecl2+H2
0,15---0,3-----------0,15
n Fe=0,15 mol
=>VH2=0,15.22,4=3,36l
2H2+O2-to>2H2O
0,15---------------0,15
n O2=0,2 mol
=>O2 dư
=>m H2O=0,15.18=2,7g