để hòa tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch hcl 2m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nZn=6,5/65=0,1mol
a, Ta có pt:Zn+2HCl--->ZnCl2+H2
b, 0,1--->0,2mol
=>thể tích HCl cần dùng là:VHCl=n/Cm=0,2/2=0,1l
Ta có pt:NaOH+HCl--->NaCl+H2
0,2<----0,2mol
mNaOH cần dùng:mNaOH=0,2.40=8g

\(Cu\left(OH\right)_2+2HCl->CuCl_2+H_2O\\ n_{Cu\left(OH\right)_2}=\dfrac{4,9}{98}=0,05< \dfrac{n_{HCl}}{2}=\dfrac{2.0,15}{2}=0,15\Rightarrow HCl:dư\left(0,05mol\right)\\ M\left(OH\right)_2+2HCl->MCl_2+H_2O\\ Có:0,228.25.1,3.2:\left(M+34\right)=0,05.36,5\\ M=-33\left(loại\right)\)
Vậy không có kim loại M thoả đề

Câu 1:
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Ta có: \(n_{HCl}=0,2\cdot2=0,4\left(mol\right)=n_{NaOH}\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
Câu 2: Bạn xem lại đề !!

\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,25 0,5 0,25
b) \(n_{H2}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,25.22,4=5,6\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
Chúc bạn học tốt
\(a,PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ b,n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ \Rightarrow n_{H_2}=0,25\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,25\cdot22,4=5,6\left(l\right)\\ c,n_{HCl}=2n_{Mg}=0,5\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,5}{2}=0,25\left(l\right)\)

a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,3<---0,6<-------------0,3
=> mZn = 0,3.65 = 19,5 (g)
b) \(V_{dd.HCl}=\dfrac{0,6}{2}=0,3\left(l\right)\)

- Thí nghiệm 1: Gọi hóa trị của X là n
CÓ n H2 = 0,06 ( mol ) => n HCL = 0,12 ( mol )
PTHH: 2X +2n HCL ===> 2XCLn + nH2
theo pthh: n X = 0,12/n ( mol )
=> X = 32,5n
Xét: n = 2 => X = 65 ( Zn )
- Thí nghiệm 2
Gọi CT của oxit : YaOb
PTHH
\(YaOb+2bHCL\rightarrow aYCl_{\dfrac{2b}{a}}+bH2O\)
theo pthh: n YaOb = 0,06/b ( mol )
=> aY + 16b = 160/3 . b
=> Y = 56 . 2b/a
Xét: 2b/a = 3 => Y = 56 ( Fe )

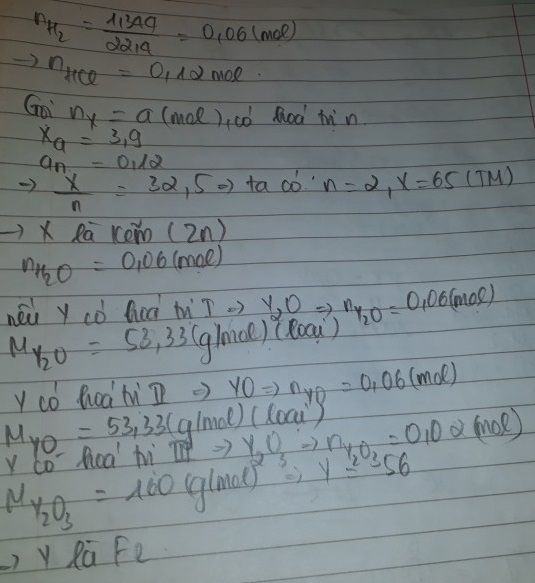
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 ( mol )
\(V_{HCl}=\dfrac{0,2}{2}=0,1l\)