Đốt cháy hoàn toàn 7,8 gam hợp chất A thu được 26,4 gam CO2 và 5,4 gam H2O.
a/ Tính % khối lượng C, H trong A.
b/ A có chứa oxi không? Tại sao?
c/ Tỉ khối hơi của A so với không khí là 2,69. Xác định CTHH của A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCO2 = 0,08 => nC = 0,08 mol
nH2O = 0,08 => nH = 0,08.2 = 0,16 mol
mX = mC + mH + mO => mO = mX - mC - mH = 1,76-0,08.12-0,16.1 =0,64 gam
nO= 0,64 : 16 = 0,04
Gọi công thức đơn giản nhất của X là CxHyOz => CTPT của X có dạng (CxHyOz )n
x:y:z = nC : nH : nO = 0,08 : 0,16 : 0,04 = 2:4:1
CTĐGN : C2H4O
Mx = 3,04.29 = 88 ==> (C2H4O)n = 88 => n =2
Vậy CTPT của X là C4H8O2

Số mol O2, CO2 và H2O đều bằng 0,3 (mol).
a/ BTKL: a+0,3.32=13,2+5,4 \(\Rightarrow\) a=9 (g).
b/ mC=n\(CO_2\).12=0,3.12=3,6 (g) \(\Rightarrow\) %mC=(3,6/9).100%=40%.
mH=2n\(H_2O\)=2.0,3=0,6 (g) \(\Rightarrow\) %mH=(0,6/9).100%\(\approx\)6,67%.
\(\Rightarrow\) %mO\(\approx\)100%-(40%+6,67%)\(\approx\)53,33%.
c/ Gọi CTHH của A là CxHyOz.
MA=7,5.4=30 (g/mol).
x:y:z=\(\dfrac{3,6}{12}:\dfrac{0,6}{1}:\dfrac{4,8}{16}=1:2:1\).
\(\Rightarrow\) CTPT của A là (CH2O)n mà MA=30 (g/mol), suy ra CTHH của A là CH2O.

Ta có: \(n_{CO_2}=\dfrac{7,04}{44}=0,16\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,16}{18}=0,12\left(mol\right)\Rightarrow n_H=0,12.2=0,24\left(mol\right)\)
\(n_{N_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\Rightarrow n_N=0,04.2=0,08\left(mol\right)\)
Ta có: mC + mH + mN = 0,16.12 + 0,24.1 + 0,08.14 = 3,28 (g) < 5,84 (g)
→ A chứa C, H, O và N.
⇒ mO = 5,84 - 3,28 = 2,56 (g) ⇒ nO = 0,16 (mol)
Gọi CTPT của A là CxHyOzNt.
⇒ x:y:z:t = 0,16:0,24:0,16:0,08 = 2:3:2:1
→ CTPT của A có dạng (C2H3O2N)n (n nguyên dương)
Mà: \(M_A< 29.3=87\Rightarrow\left(12.2+3+16.2+14\right)n< 87\)
\(\Rightarrow n< 1,2\Rightarrow n=1\)
Vậy: CTPT của A là C2H3O2N.

a)
$n_C = n_{CO_2} = \dfrac{4,4}{44} = 0,1(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{1,8}{18} = 0,2(mol)$
$\Rightarrow n_O = \dfrac{2,2 - 0,1.12 - 0,2.1}{16} = 0,05(mol)$
$n_C : n_H : n_O = 0,1 : 0,2 : 0,05 = 2 : 4 : 1$
Vậy CTĐGN là $C_2H_4O$
b)
CTPT của A là $(C_2H_4O)_n$
Ta có:
$M_A = (12.2 + 4 + 16)n = 22.2 \Rightarrow n = 1$
Vậy CTPT của A là $C_2H_4O$
\(n_{CO_2}=\dfrac{4.4}{44}=0.1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_O=2.2-0.1\cdot12-0.1\cdot2=0.8\left(g\right)\)
\(n_O=\dfrac{0.8}{16}=0.05\left(mol\right)\)
\(n_C:n_H:n_O=0.1:0.2:0.05=2:4:1\)
CT đơn giản nhất : \(C_2H_4O\)
\(M_A=22\cdot2=44\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow44n=44\)
\(\Leftrightarrow n=1\)
\(A:C_2H_4O\)

n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
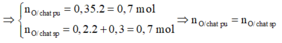
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
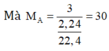
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.

1) Bảo toàn C: \(n_C=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn H: \(n_H=\dfrac{10,8}{18}.2=1,2\left(mol\right)\)
Bảo toàn O: \(n_O=\dfrac{9,2-0,4.12-1,2}{16}=0,2\left(mol\right)\)
\(M_A=23.2=46\left(\dfrac{g}{mol}\right)\)
CTPT: CxHyOz
=> x : y : z = 0,4 : 1,2 : 0,2 = 2 : 6 : 1
=> (C2H6O)n = 46
=> n = 1
CTPT: C2H6O
CTCT:
(1) CH3-CH2-OH
(2) CH3-O-CH3
2) Ta có:
\(V_{C_xH_y}:V_{O_2}:V_{CO_2}=1:6:4\)
=> \(n_{C_xH_y}:n_{O_2}:n_{CO_2}=1:6:4\)
Bảo toàn C: \(x=n_C=n_{CO_2}=4\left(mol\right)\)
Bảo toàn O: \(n_{O\left(H_2O\right)}=2n_{O_2}-2n_{CO_2}=2.6-2.4=4\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2n_{O\left(H_2O\right)}=2.4=8\left(mol\right)\)
=> Trong 1 mol A chứa 4 mol C và 8 mol H
=> CTPT: C4H8
CTCT:
(1) CH2=CH-CH2-CH3
(2) CH3-CH=CH-CH3
\(\left\{{}\begin{matrix}n_H=2.\dfrac{5,4}{18}=0,6\left(mol\right)\\n_C=\dfrac{26,4}{44}=0,6\left(mol\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}m_H=0,6.1=0,6\left(g\right)\\m_C=0,6.12=7,2\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_H=\dfrac{0,6}{7,8}=7,7\%\\\%m_C=\dfrac{7,2}{7,8}=92,3\%\end{matrix}\right.\)\
Xét 0,6 + 7,2 = 7,8 => A chỉ có C và H
\(CTPT:C_aH_b\\ \rightarrow a:b=0,6:0,6=1:1\\ \rightarrow\left(CH\right)_n=2,69.29=78\\ \rightarrow n=6\\ CTPT:C_6H_6\left(benzen\right)\)