Sục từ từ V lít khí CO2 (đktc) vào 300ml dung dich chứa Ba(OH)2 0,1 M và KOH 0,2 M thu được 5,91 gam kết tủa. Tính V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{Ba\left(OH\right)_2}=0,5.1=0,5\left(mol\right)\)
\(n_{KOH}=0,5.2=1\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{39,4}{197}=0,2\left(mol\right)\)
TH1: Kết tủa chưa bị hòa tan.
PT: \(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
_____0,2_________________0,2 (mol)
\(\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
TH2: Kết tủa đã bị hòa tan 1 phần.
PT: \(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
_____0,5______0,5________0,5 (mol)
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,5________1________0,5 (mol)
\(CO_2+H_2O+K_2CO_3\rightarrow2KHCO_3\)
0,5_____________0,5 (mol)
\(CO_2+BaCO_3+H_2O\rightarrow Ba\left(HCO_3\right)_2\)
0,3________0,3 (mol)
\(\Rightarrow V_{CO_2}=\left(0,5+0,5+0,5+0,3\right).22,4=40,32\left(l\right)\)
\(n_{Ba\left(OH\right)_2}=0,5.1=0,5\left(mol\right)\)
\(n_{KOH}=2.0,5=1\left(mol\right)\)
\(n_{Ba_2CO_3}=\dfrac{39,4}{137}\left(mol\right)\)
PTHH :
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
39,4/137 39,4/137 39,4/137
Ba(OH)2 dư nên không phản ứng tiếp .
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
1 0,5
\(V_{CO_2}=\left(\dfrac{197}{685}+0,5\right).22,4\approx17,64\left(l\right)\)


+) Trường hợp 2: Kết tủa sau khi đạt giá trị tối đa bị hòa tan một phần:
Khi đó
![]()
![]()
Đáp án A.

Đáp án D
Lượng CO 2 tham gia phản ứng và lượng Ba ( OH ) 2 ở hai thí nghiệm đều bằng nhau, nhưng ở TN1 thu được lượng kết tủa ít hơn ở TN2. Suy ra ở TN1 kết tủa đã bị hòa tan một phần. Dựa vào tính chất của đồ thị ở TN1 suy ra :
n CO 2 = 2 n Ba ( OH ) 2 - n BaCO 3 = ( 2 a - 0 , 1 ) mol
Đồ thị biểu diễn sự biến thiên lượng kết tủa theo lượng CO 2 ở TN1 và TN2 :
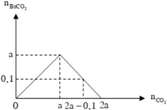
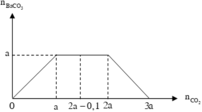
Dựa vào 2 đồ thị, ta thấy a < 2a - 0,1 < 2a nên ở TN2 kết tủa đạt cực đại. Suy ra :
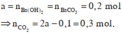
Vậy V = 6,72 lít và a = 0,2 mol

Đáp án B
nCO2= 3,36 : 22,4 = 0,15 (mol);
nNaOH = 0,2 ; nKOH = 0,1 (mol) => ∑ nOH- = 0,3 (mol)
Ta có: nOH-/ nCO2 = 0,3/ 0,15 = 2 => chỉ tạo muối trung hòa
CO2 + 2OH- → CO32- + H2O
0,15 0,3 → 0,15
Vậy dd X gồm : K+, Na+ ; CO32- : 0,15 (mol)
Dd X + Ba(OH)2: 0,2 (mol) có phản ứng
Ba2+ + CO32- → BaCO3↓
0,15← 0,15 →0,15 (mol)
=> mBaCO3 = 0,15. 197 = 29,55 (g)

\(n_{Ca\left(OH\right)_2}=0,32\left(mol\right)\)
\(n_{KOH}=0,6\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
PTHH :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,1 0,32 0,1
Ca(OH)2 dư nên tính theo CaCO3
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,3 0,6
\(V_{CO_2}=\left(0,1+0,3\right).22,4=8,96\left(l\right)\)

Đáp án A
Theo giả thiết ta có :
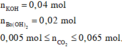
Dựa vào bản chất phản ứng và giả thiết, ta có đồ thị :
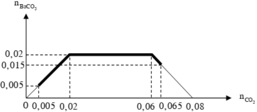
Khi 0 , 005 mol ≤ n CO 2 ⩽ 0 , 065 mol thì lượng kết tủa biến thiên theo đường nét đậm trên đồ thị. Điểm cực đại là 0,02 và cực tiểu là 0,005.
Suy ra : 0,985 gam ≤ m BaCO 3 ≤ 3,94 gam

Đáp án C
Trường hợp 1: Thí nghiệm ban đầu chưa có phản ứng hòa tan một phần kết tủa
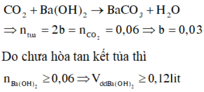
Trường hợp 2: Thí nghiệm ban đầu đã có phản ứng hòa tan hoàn toàn kết tủa
Áp dụng công thức giải nhanh
Thí nghiệm 1 có 2b = 0,5V - 0,06
Thí nghiệm 2 có b = 0,5V - 0,08
![]()
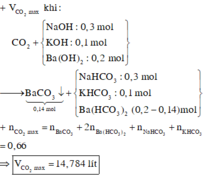
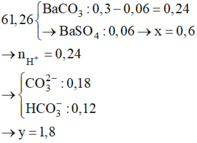
\(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,1.0,3=0,03\left(mol\right)\\n_{KOH}=0,2.0,3=0,06\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3}=\dfrac{5,91}{197}=0,03\left(mol\right)\)
Do nBaCO3 = nBa(OH)2 => Ba2+ bị kết tủa hết
PTHH:
(1) Ba(OH)2 + CO2 --> BaCO3 + H2O
(2) 2NaOH + CO2 --> Na2CO3 + H2O
(3) Na2CO3 + CO2 + H2O --> 2NaHCO3
- Nếu CO2 chỉ tham gia vào pư (1)
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03<---0,03
=> nCO2(min) = 0,03 (mol) (*)
- Nếu CO2 tham gia vào pư (1), (2), (3)
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03----->0,03----->0,03
2NaOH + CO2 --> Na2CO3 + H2O
0,06--->0,03------>0,03
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,03---->0,03
=> nCO2(max) = 0,09 (mol) (**)
(*)(**) => \(0,03\le n_{CO_2}\le0,09\)
=> \(0,672\le V\le2,016\)