0,24 mol clo và 0,26 mol oxi phản ứng hết với 16,98g hỗn hợp gồm Mg và Al. khối lượng Mg và Al trong hỗn hợp là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\left\{{}\begin{matrix}Cl_2:x\left(mol\right)\\O_2:y\left(mol\right)\end{matrix}\right.\)
\(BTe:3n_{Al}+2n_{Mg}=2n_{Cl_2}+4n_{O_2}\)
\(\Rightarrow2x+4y=3\cdot0,2+0,1\cdot2=0,8\left(1\right)\)
\(BTKL:m_{muối}=m_{Al^{3+}}+m_{Mg^{2+}}+m_{Cl^-}+m_{O^{2-}}\)
\(\Rightarrow25,2=0,2\cdot27+0,1\cdot24+35,5\cdot2x+16\cdot2y\)
\(\Rightarrow71x+32y=17,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1mol\\y=0,1mol\end{matrix}\right.\)
\(V=V_{Cl_2}+V_{O_2}=0,1\cdot22,4+0,1\cdot22,4=4,48l\)
Chọn D

n Mg = 3,6/24 = 0,15(mol)
n Al = 5,4/27 = 0,2(mol)
Gọi n Cl2 = a(mol) ; n O2 = b(mol)
Bảo toàn e :
2n Cl2 + 4n O2 = 2n Mg + 3n Al
<=> 2a + 4b = 0,15.2 + 0,2.3 = 0,9(1)
Bảo toàn khối lượng :
m X + m Al + m Mg = m Z
=> 71a + 32b = 29,95 - 3,6 -5,4 = 20,95(2)
Từ (1)(2) suy ra a = 0,25 ; b = 0,1
%m O2 = 0,1.32/(0,25.71 + 0,1.32) .100% = 15,27%

Chọn C. Đặt nCl2=x mol và nO2=y mol. Phản ứng vừa đủ tạo muối gồm các ion sau: Al3+, Mg2+ , Cl- , O2-.
Theo định luât bảo toàn điện tích: 3nAl3+ +2nMg2+ = nCl- + 2nO2- = 2nCl2 + 4nO2
mmuối= 27nAl3+ +24nMg2+ + 35,5nCl- + 16nO2-
→ Hệ
3 . 0 , 2 + 2 . 0 , 1 = 2 x + 4 y 27 . 0 , 2 + 24 . 0 , 1 + 71 x + 32 y = 25 , 2 → x = 0 , 2 y = 0 , 1

Giải thích:
- Theo đề bài ta có :
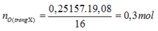
- Khi cho dung dịch tác dụng với NaOH dư ta được :
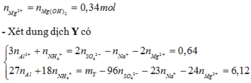
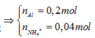
- Quy đổi hỗn hợp rắn X thành Mg, Al, O và C. → bảo toàn C
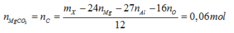
- Quay lại hỗn hợp rắn X với Al, Al2O3, Mg và MgCO3 có :
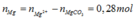
Bảo toàn O
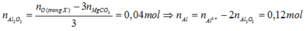
- Xét hỗn hợp khí Z ta có : nN2O = a và nH2 = b và nCO2 = 0,06 mol
→ MZ = 30 = (44a + 2b + 0,06.44) : (a + b +0,06)
Bảo toàn e cho phản ứng với HNO3 có 8nN2O + 2nH2 + 8nNH4+ = 3nAl + 2nMg
→ a = 0,06 và b =0,06 mol
- Xét toàn bộ quá trình phản ứng của X với dung dịch chứa 1,32 mol NaHSO4 và x mol HNO3 có:
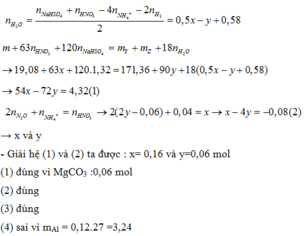
Đáp án C


Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
⇒ 24x + 27y = 16,98 (1)
Các quá trình:
\(Mg^0\rightarrow Mg^{+2}+2e\)
x_____________2x (mol)
\(Al^0\rightarrow Al^{+3}+3e\)
y___________3y (mol)
\(Cl_2^0+2e\rightarrow2Cl^-\)
0,24_0,48 (mol)
\(O_2^0+4e\rightarrow2O^{-2}\)
0,26_1,04 (mol)
Theo ĐLBT e, có: 2x + 3y = 0,48 + 1,04 ⇒ 2x + 3y = 1,52 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,55\left(mol\right)\\y=0,14\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,55.24=13,2\left(g\right)\\m_{Al}=0,14.27=3,78\left(g\right)\end{matrix}\right.\)
Bạn tham khảo nhé!