Đốt cháy 26,3 gam hỗn hợp Cu và Al trong không khí (dư) thu được 41,5 gam hỗn hợp CuO và Al2O3.
a/ Viết PTHH của phản ứng xảy ra.
b/ Tính thể tích không khí (đktc) đã phản ứng (biết O2 chiếm 20% thể tích không khí)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

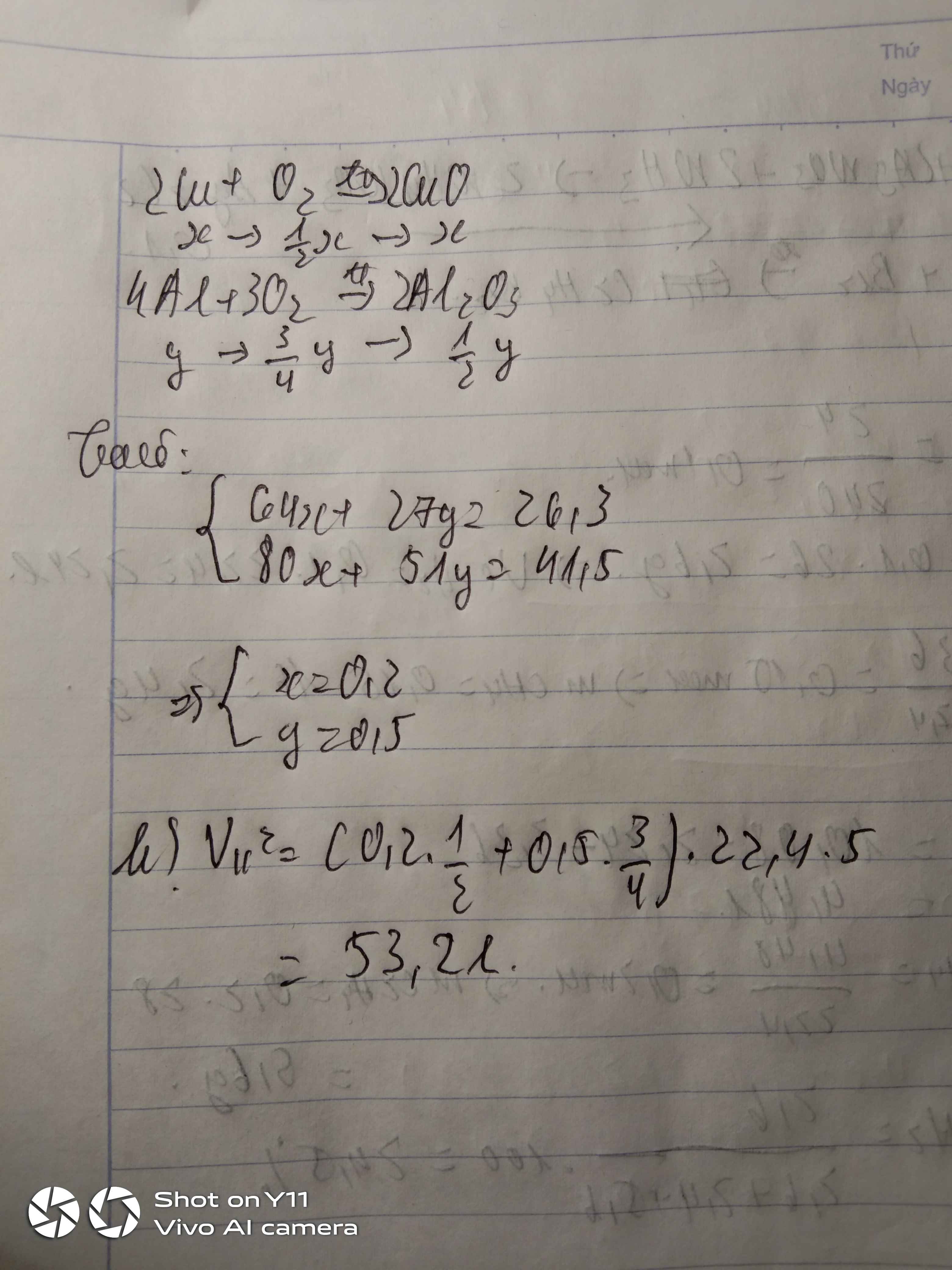

a.
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\) \(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
x 1/2x x y 3/4y 1/2y ( mol )
Gọi \(\left\{{}\begin{matrix}n_{Cu}=x\\n_{Al}=y\end{matrix}\right.\)
Ta có:
\(\left\{{}\begin{matrix}64x+27y=26,3\\80x+\dfrac{1}{2}y.102=41,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,5\end{matrix}\right.\)
\(V_{kk}=\left(\dfrac{1}{2}.0,2+\dfrac{3}{4}.0,5\right).22,4.5=0,475.112=53,2l\)

a: \(4Al+3O_2\rightarrow2Al_2O_3\)
b: \(n_{Al}=\dfrac{21.6}{27}=0.8\left(mol\right)\)
\(\Leftrightarrow n_{Al_2O_3}=0.4\left(mol\right)\)
\(m_{Al_2O_3}=0.4\cdot102=40.8\left(g\right)\)
c: \(n_{O_2}=0.6\left(mol\right)\)
\(V_{O_2}=0.6\cdot22.4=13.44\left(lít\right)\)
a) 4Al + 3O2 --to--> 2Al2O3
b) \(n_{Al}=\dfrac{21,6}{27}=0,8\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,8-->0,6-------->0,4
=> \(m_{Al_2O_3}=0,4.102=40,8\left(g\right)\)
c) \(V_{O_2}=0,6.22,4=13,44\left(l\right)\)
d) \(V_{kk}=13,44:20\%=67,2\left(l\right)\)

a) \(4Al+3O_2-^{t^o}\rightarrow2Al_2O_3\)
Bảo toàn khối lượng : \(m_{O_2}=12,24-8,1=4,14\left(g\right)\)
=>\(n_{O_2}=\dfrac{207}{1600}\left(mol\right)\)
Vì O2 chiếm 20% thể tích không khí
\(V_{kk}=\dfrac{\dfrac{207}{1600}.22,4}{20\%}=14,49\left(lít\right)\)
b) \(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
Lập tỉ lệ : \(\dfrac{0,3}{4}>\dfrac{\dfrac{207}{1600}}{3}\)
=> Sau phản ứng Al dư
\(n_{Al\left(pứ\right)}=\dfrac{207}{1600}.\dfrac{4}{3}=0,1725\left(mol\right)\)
=> \(H=\dfrac{0,1725}{0,3}.100=57,5\%\)
c) D gồm Al2O3 và Al dư
\(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=\dfrac{69}{800}\left(mol\right);n_{Al\left(dư\right)}=0,3-0,1725=0,1275\left(mol\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Sigma n_{HCl}=\dfrac{69}{800}.6+0,1275.3=0,9\left(mol\right)\)
=> \(m_{HCl}=0,9.36,5=32,85\left(g\right)\)

Đáp án A
12(g) Kim loại + ?O2 ® 16(g) Oxit.
Bảo toàn khối lượng: mO2 = 4(g) ⇒ nO2 = 0,125 mol.
||⇒ VO2 = 0,125 × 22,4 = 2,8 lít

\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2|\)
2 2 2 2 3
0,2 0,2 0,3
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O|\)
1 2 2 1
0,1 0,2
b) \(n_{Al}=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Al2O3}=15,6-5,4=10,2\left(g\right)\)
c) Có : \(m_{Al2O3}=10,2\left(g\right)\)
\(n_{Al2O3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
\(n_{NaOH\left(tổng\right)}=0,2+0,2=0,4\left(mol\right)\)
\(V_{ddNaOH}=\dfrac{0,4}{1}=0,4\left(l\right)=400\left(ml\right)\)
Chúc bạn học tốt

Chọn đáp án C
Bảo toàn khối lượng:
n C l 2 = 20 , 15 - 5 , 95 71 = 0,2 (mol)
=> V = 0,2.22,4 = 4,48 (lít)

Đáp án : A
Áp dụng định luật bảo toàn khối lượng => mCl2 = m muối – m kim loại = 40,3 – 11,9 = 28,4g
=> nCl2 = 0,4 mol = > V = 8,96 lít