2.2) Khi hòa tan m gam kim loại nhôm vào dung dịch HCl dư thấy V1 lít khí H2(đktc). Nếu cũng lấy m gam kim loại M tác dụng HCl dư thoát ra V2 lít H2(ĐKTC). Biết V1=3,06V2. Tìm kim loại M?
GIÚP T VỚI Ạ!!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi M có số oxi hóa từ 0 lên +n
BT e: ta có: 8,1n/ M = 10,08. 2/ 22,4
Tìm được M = 9n.
Cặp nghiệm thỏa mãn là n= 3 và M= 27 (Al)
+ Al có thể tác dụng với dd HCl và NaOH
+ Al được điều chế bằng phương pháp điện phân nóng chảy
+ Độ dẫn điện của Al < Cu
+ Al là kim loại nhẹ ( 2,7 g/ cm^3)

Đáp án A
Gọi M có số oxi hóa từ 0 lên +n
BT e: ta có: 8,1n/ M = 10,08. 2/ 22,4
Tìm được M = 9n.
Cặp nghiệm thỏa mãn là n= 3 và M= 27 (Al)
+ Al có thể tác dụng với dd HCl và NaOH
+ Al được điều chế bằng phương pháp điện phân nóng chảy
+ Độ dẫn điện của Al < Cu
+ Al là kim loại nhẹ ( 2,7 g/ cm^3)

Đáp án B.
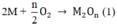
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
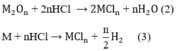
Số mol H2: 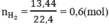
Theo phương trình (1)
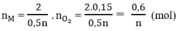
Theo phương trình (3)
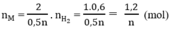
Tổng số mol M là 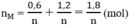
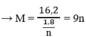
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al

\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)

\(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(n_{M\left(pu\right)}=a\left(mol\right)\)
Bảo toàn e :
\(na=0.15\cdot4+0.6\cdot2=1.8\)
\(a=\dfrac{1.8}{n}\)
\(M=\dfrac{16.2}{\dfrac{1.8}{n}}=9n\)
\(n=3\Rightarrow M=27.M:Al\)
Đặt m = 27 gam → nAl = 1 mol
2Al + 6HCl → 2AlCl3 + 3H2
1 1,5 mol
khối lượng của nhôm và kim loại M bằng nhau → mM = 27 gam
V1 = 3,06 V2 → nH2 (Al) = 3,06.nH2 (M)
→ nH2 (M) = 1,5/3,06 = 0,49 mol
PT: 2M + 2nHCl → 2MCln + nH2
0,98/n 0,49
nM = 0,98/n mol, mM = 27 gam
→ M = \(\dfrac{27n}{0,98}\) ≃ 27,55n
Xét n = 1 → M = 27,55 (loại)
n = 2 → M = 55,1 → M là Mangan (Mn)