Glixerol là chất được pha thêm vào cồn để làm nước rửa tay sát khuẩn, giúp cho da tay không bị khô. Glixerol được tạo bởi cacbon, hidro và oxi với % khối lượng tương ứng là 39,13%%, 8,7%, còn lại là oxi. Tìm công thức chất này biết phân tử chất này nặng gấp 2 lần phân tử khí NO2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

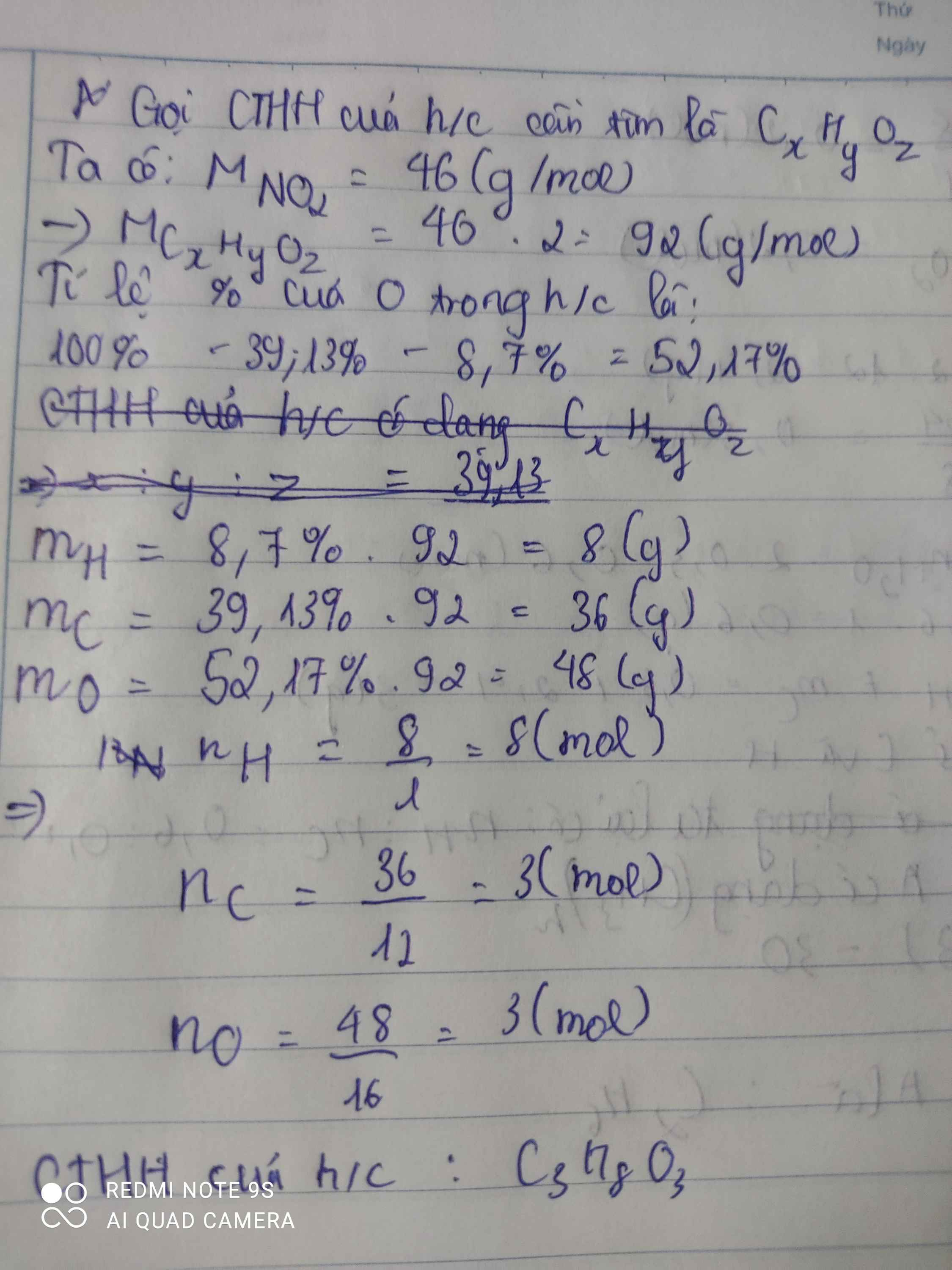

CTC: CxHyOz
\(Theo.đề.bài.ta.có:\)
\(x:y:z=\dfrac{76,92}{12}:\dfrac{12,82}{1}:\dfrac{10,26}{16}=6,41:12,82:0,64125\)
\(x:y:z=10:20:1\)
\(Vì.chất.này.có.phân.tử.nhỏ.hơn.\)166g/mol
\(\Rightarrow C_{10}H_{20}O\)
< Cái này ba chỉ mình làm, nếu cách làm chưa được thì bạn thông cảm nhé >

a) \(M_{axit.malic}=\dfrac{67}{0,5}=134\left(g/mol\right)\)
b) \(d_{axit.malic/H_2}=\dfrac{134}{2}=67\)
c) \(m_C:m_H:m_O=35,82\%:4,48\%:59,7\%\)
=> \(n_C:n_H:n_O=\dfrac{35,82}{12}:\dfrac{4,48}{1}:\dfrac{59,7}{16}=4:6:5\)
=> CTPT: (C4H6O5)n
Mà M = 134
=> n = 1
=> CTPT: C4H6O5
d) Gọi số mol (NH2)2CO là a (mol)
=> nH = 4a (mol) (1)
\(n_{C_4H_6O_5}=\dfrac{40,2}{134}=0,3\left(mol\right)\)
=> nH = 1,8 (mol) (2)
(1)(2) => a = 0,45 (mol)
=> \(m_{\left(NH_2\right)_2CO}=0,45.60=27\left(g\right)\)

Gọi CTHH là \(C_xH_yO_z\)
\(\%m_O=100\%-\left(35,82\%+4,48\%\right)=59,7\%\)
\(x:y:z=\dfrac{\%m_C}{12}:\dfrac{\%m_H}{1}:\dfrac{\%m_O}{16}=\dfrac{35,82\%}{12}:\dfrac{4,48\%}{1}:\dfrac{59,7\%}{16}\)
\(=0,02985:0,0448:0,0373125=1:1,5:1,25\)
\(=4:6:5\)
Vậy CTHH là \(C_4H_6O_5\)

(1). Chất béo nhẹ hơn nước, khôngtan trong nước nhưng tan trong các dung môi hữu cơ không phân cực.
(2). Chất béo là trieste của glixerol với cácaxit béo
(4). Tristearin có nhiệt độnóng chảycao hơn nhiệt độ nóng chảycủa triolein
(5). Hidro hóa hoàn toàn triolein hoặc trilinolein đều thu được tristearin.
(7). Dầu mỡ động thực vật bị ôi thiu do nối đôi C = C ở gốc axit không no của chất béo bị oxi hóa chậm bởi oxi không khí tạo thành peoxit, chất này bị phân hủy thành các sản phẩm có mùi khó chịu.
(8). Chất béo nhẹ hơn nước và không tan trong nước.
(9). Thành phần nguyên tố của chất béo rắn giống với dầu ăn.
đáp án B

Đáp án B
X có ít nhất 3π, đốt X và Y cho n CO2 = nH2O = 0,7 mol nên Y phải là ancol no.
Giả sử X có kπ thì đốt X cho nCO2 – nH2O = (k-1).nX, đốt Y có nCO2 – nH2O = – nY
mà nY = 5nX → k – 1 = 5 → k = 6. Vậy X có 3 liên kết π trong C = C (do đã có sẵn 3π trong chức este – COO).
Do đó, khi cho E tác dụng Br2 thì chỉ xảy ra: X + 3Br2 → sp. → nX = 0,02 mol. ↔ nY = 0,1 mol.
Gọi số C của X và Y tương ứng là n, m ta có nCO2 = 0,02 × n + 0,1 × m = 0,7 mol ↔ n + 5m = 35.
Để ý số C ít nhất của X phải > 6 → m ≤ 5, Y lại có mạch C phân nhánh ↔ m ≥ 4 → m = 4 hoặc m = 5.
Mà Y không tách được nước tạo anken → duy nhất 1 công thức thỏa mãn là
ancol 2,2-đimetylpropan-1-ol ↔ C5H12O → n = 10 ↔ X là: C10H10O6
% mY ≈ 66,07 %.