Hòa tan hết 12,8g hỗn hợp gồm Fe và FeO bằng dd HCl 2M. Sau phản ứng thu được 2,24 lít khí (đktc). Tính a. Thành phần% về khối lượng của mỗi chất có trong hỗn hợp. b. Thể tích dung dịch HCl cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2<---0,6<--------------0,3
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{0,2.27}{15,6}.100\%=34,615\%\\\%Al_2O_3=\dfrac{15,6-0,2.27}{15,6}.100\%=65,385\%\end{matrix}\right.\)
b) \(n_{Al_2O_3}=\dfrac{15,6-0,2.27}{102}=0,1\left(mol\right)\)
PTHH: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
______0,1--->0,6
=> nHCl = 0,6+0,6 = 1,2(mol)
=> \(V_{dd}=\dfrac{1,2}{2}=0,6\left(l\right)\)

nH2 = 2.24/22.4 = 0.1 (mol)
Fe + 2HCl => FeCl2 + H2
0.1___0.2_____0.1___0.1
mFeO = 12.8 - 0.1*56 = 7.2 (g)
nFeO = 7.2/72 = 0.1 (mol)
FeO + 2HCl => FeCl2 + H2O
0.1____0.2______0.1
%Fe = 5.6/12.8 * 100% = 43.75%
%FeO = 56.25%
nHCl = 0.2 + 0.2 = 0.4 (mol)
Vdd HCl = 0.4/0.1 = 4(l)
nFeCl2 = 0.1 + 0.1 = 0.2 (mol)
CM FeCl2 = 0.2/4 = 0.05 (M)

a, Ta có: 24nMg + 56nFe = 12,8 (1)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Mg}+n_{Fe}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,3\left(mol\right)\\n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,3.24=7,2\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
b, \(n_{HCl}=2n_{H_2}=0,8\left(mol\right)\)
\(\Rightarrow V_{HCl}=\dfrac{0,8}{2}=0,4\left(l\right)\)
c, \(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Theo PT: \(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=n_{MgCl_2}=n_{Mg}=0,3\left(mol\right)\\n_{Fe\left(OH\right)_2}=n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{\downarrow}=0,3.58+0,1.90=26,4\left(g\right)\)
a. Số gam mỗi kim loại trong hỗn hợp ban đầu:
Mg: 9,6 gamFe: 22,4 gamb. Thể tích dung dịch HCl 2M đã phản ứng: 0,2 lít
c. Khối lượng kết tủa thu được khi dd A tác dụng với dung dịch NaOH dư là 0,4 gam.
------------------------------------đấy

Tiếp bài của creeper nhé:
c. Ta có: \(n_{ZnO}=\dfrac{4,86}{81}=0,06\left(mol\right)\)
Theo PT(1): \(n_{HCl}=2.n_{ZnO}=2.0,06=0,12\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{Zn}=2.0,1=0,2\left(mol\right)\)
=> \(n_{HCl}=0,12+0,2=0,32\left(mol\right)\)
=> \(m_{HCl}=0,32.36,5=11,68\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{11,68}{m_{dd_{HCl}}}.100\%=12\%\)
=> \(m_{dd_{HCl}}=\dfrac{292}{3}\left(g\right)\)
Theo đề, ta có:
\(D=\dfrac{\dfrac{292}{3}}{V_{dd_{HCl}}}=1,2\)(g/ml)
=> \(V_{dd_{HCl}}=81,1\left(ml\right)\)

a)
$Fe + 2HCl \to FeCl_2 + H_2$
$FeO + 2HCl \to FeCl_2 + H_2O$
b)
Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
$m_{FeO} = 12 - 8,4 = 3,6(gam)$
$n_{FeO} =0,05(mol)$
Theo PTHH : $n_{HCl} = 2n_{Fe} + 2n_{FeO} = 0,4(mol)$
$V_{dd\ HCl} = \dfrac{0,4}{2} = 0,2(lít)$
c) $Fe + CuSO_4 \to FeSO_4 + Cu$
$n_{Cu} = n_{Fe} = 0,15(mol) \Rightarrow m_{chất\ rắn} = m_{FeO} + m_{Cu}$
$= 3,6 + 0,15.64 = 13,2(gam)$

a,\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,1 0,2 0,1 0,1
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Fe}=0,1.56=5,6\left(g\right);m_{Fe_2O_3}=13,6-5,6=8\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
b,\(m_{HCl}=\left(0,2+0,3\right).98=49\left(g\right)\)
\(m_{ddHCl}=\dfrac{49.100}{10}=490\left(g\right)\)
c,\(m_{ddX}=13,6+490-0,1.2=503,4\left(g\right)\)
d,\(C\%_{FeCl_2}=\dfrac{0,1.127.100\%}{503,4}=2,52\%\)
\(C\%_{FeCl_3}=\dfrac{0,05.162,5.100\%}{503,4}=1,614\%\)
mik nhầm C%FeCl3
Sửa lại: \(C\%_{FeCl_3}=\dfrac{0,1.162,5.100\%}{503,4}=3,228\%\)

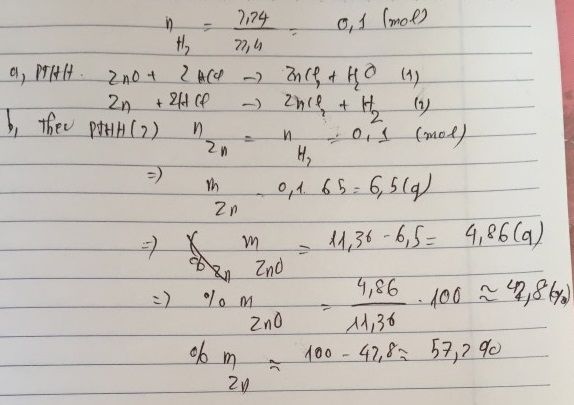

Fe + 2HCl -> FeCl2 + H2
0.2 0.1
FeO + 2HCl -> FeCl2 + H2O
0.1 0.2
a.\(nH2=\dfrac{2.24}{22.4}=0.1mol\)
\(\%mFe=\dfrac{0.1\times56\times100}{12.8}=43.8\%\)
\(\%mFeO=100-43.8=56.2\%\)
b.\(nFeO=\dfrac{12.8-\left(0.1\times56\right)}{56+16}=0.1mol\)
\(V_{HCl}=\dfrac{0.2+0.2}{2}=0.2l\)