hổn hợp khí X gồm O3(OZON) và O2 có tỉ khối hơi đối với H2 bằng 20. tính % theo thể tích mỗi khí trong X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO

Chọn đáp án C
Sử dụng sơ đồ đường chéo ⇒ nO2:nO3 = 5:3
+ Giả sử nCO2 6 mol và nH2O = 7 mol ta có sơ đồ.
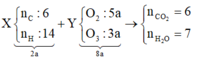
+ Bảo toàn Oxi ⇒ 2nO2 + 3nO3 = 5x2a + 3x3a = 2nCO2 + nH2O = 6x2 + 7 = 19 ⇒ a = 1
![]()
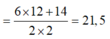
⇒ Chọn C

Chọn đáp án C
Sử dụng sơ đồ đường chéo ⇒ nO2:nO3 = 5:3
+ Giả sử nCO2 6 mol và nH2O = 7 mol ta có sơ đồ.
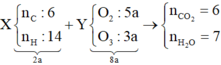
+ Bảo toàn Oxi ⇒ 2nO2 + 3nO3 = 5x2a + 3x3a = 2nCO2 + nH2O = 6x2 + 7 = 19 ⇒ a = 1
![]()
⇒ Chọn C

Đáp án A.
Coi số mol hỗn hợp X = 1 mol
n O 2 = X , n O 3 = Y ( m o l )
→ x + y = 1 32 x + 48 y = 1 . 19 , 2 . 2
→ x = 0,6 , y = 0,4 (mol)
→ % V O 2 = 60 % , % V O 3 = 40 %

ta có dhh/H2=6--->Mtrung bình hỗ hợp khí =6*2=12
bạn dùng sơ đồ đường chéo mk làm mẫu phần a kau còn lại tương tự nha
nN2 (28) 12-2=10
nH2 (2) 12 28-12=16 ta có % thể tich = % về sô mol ----> %Vh2=\(\frac{16}{10+16}\)=61,5 %( xấp xỉ nha) %VN2 = 100-61,5=38,5%

a) Gọi nO2 =a (mol); nO3 = b(mol)
Có: \(\dfrac{32a+48b}{a+b}=20.2=40\)
=> 32a + 48b = 40a + 40b
=> 8a = 8b => a = b
=> \(\left\{{}\begin{matrix}\%V_{O_2}=\dfrac{a}{a+b}.100\%=\dfrac{a}{a+a}.100\%=50\%\\\%V_{O_3}=100\%-50\%=50\%\end{matrix}\right.\)
b) Gọi nN2 =a (mol); nNO = b(mol)
Có: \(\dfrac{28a+30b}{a+b}=14,75.2=29,5\)
=> 28a + 30b = 29,5a + 29,5b
=> 1,5a = 0,5b
=> 3a = b
=> \(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{a}{a+b}.100\%=\dfrac{a}{a+3a}.100\%=25\%\\\%V_{NO}=100\%-25\%=75\%\end{matrix}\right.\)
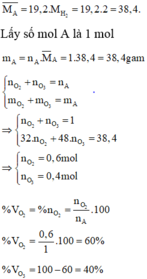

Gọi số mol O3 và O2 là a, b (mol)
Có: \(\dfrac{48a+32b}{a+b}=20.2=40\)
=> a = b
=> \(\left\{{}\begin{matrix}\%O_3=\dfrac{a}{a+b}.100\%=50\%\\\%O_2=\dfrac{b}{a+b}.100\%=50\%\end{matrix}\right.\)
MX=20.2=40g/mol
\(\left\{{}\begin{matrix}O_3=48\\O_2=32\end{matrix}\right.40\left\{{}\begin{matrix}nO_3=8\\nO_2=8\end{matrix}\right.\)
\(\dfrac{nO_3}{nO_2}=\dfrac{8}{8}=1\Rightarrow nO_3:nO_2=1:1\)
\(\Rightarrow\%O_3=50\%\\ \%O_2=50\%\)