Cho Al vào dung dịch HNO3 vừa đủ phản ứng thu được 0,9 mol N2O. Tìm số mol Al bị oxi hóa A. 2,7 mol B. 2,4 mol C. 1,8 mol D. 0,9 mol
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khôi lương muôi nitrat kim loai = 6 + 0,02 x 8 x 62 + 0,02 x 3 x 62 = 19,64 gam
-> m NH4NO3 = 25,4 - 19,64 = 5,76 gam
-> n NH4NO3 = 5,76/80 = 0,072 mol
-> n HNO3 bị khử = 2n N2O + n NO + n NH4NO3 = 0,132
=> Đáp án D

QT cho e :
Al→ Al3++ 3e (1)
QT nhận e:
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 0,3 ← 0,03 mol
NO3-+ 3e + 4H+→ NO+ 2H2O (4)
0,06 0,08← 0,02
Theo bán phản ứng (3) và (4) ta có:
nH+= 10.nN2O+ 4.nNO= 10.0,03 + 4.0,02= 0,38 mol≠ 0,58 mol
Do đó còn có thêm quá trình nhận e tạo NH4+
NO3-+ 8e + 10H+ → NH4+ + 3H2O (5)
0,16 ← 0,2
nH+ pt5= 0,58- 0,38= 0,2 mol
Theo bán phản ứng (3), (4), (5) ta có:
ne nhận= 8. nN2O+ 3.nNO+ 8/10.nH+= 0,24+ 0,06+ 0,16= 0,46 mol
Theo ĐL bảo toàn e : ne cho= ne nhận= 0,46 mol → nAl= 0,46/3 mol
→mAl= 4,14 gam
Đáp án D

\(1.3NaOH+H_3PO_4\rightarrow Na_3PO_4+3H_2O\\ a=n_{H_3PO_4}=\dfrac{1}{3}n_{NaOH}=\dfrac{1}{3}\cdot0,9=0,3mol\\ \Rightarrow A\\ 2.n_{Ba\left(OH\right)_2}=0,2.0,4=0,08mol\\ n_{H_2SO_4}=0,25.0,3=0,075mol\\ Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\\ \Rightarrow\dfrac{0,08}{1}>\dfrac{0,075}{1}\Rightarrow Ba\left(OH\right)_2.dư\\ n_{BaSO_4}=n_{H_2SO_4}=0,075mol\\ m_{\uparrow}=m_{BaSO_4}=0,075.233=16,725g\\ \Rightarrow?:))\\ 3.n_{KOH}=0,2.1=0,2mol\\ n_{H_2SO_4}=0,2.1=0,2mol\\ 2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\\ \Rightarrow\dfrac{0,2}{2}< \dfrac{0,2}{1}\Rightarrow H_2SO_4.dư\\ n_{H_2SO_4.pư}=\dfrac{1}{2}n_{KOH}=\dfrac{1}{2}\cdot0,2=0,1mol\\ n_{H_2SO_4_4.dư}=0,2-0,1mol\\ H_2SO_4+Mg\rightarrow MgSO_4+H_2\\ n_{H_2}=n_{H_2SO_4.dư}=0,1mol\\ V_{H_2}=0,1.24,79=2,479l\\ \Rightarrow A\)

Đây là dạng bài tập cho biết số mol các sản phẩm khí và khối lượng muối thu được sau phản ứng. Do đó cũng như bài trước, ta cần kiểm tra xem các sản phẩm có tạo thành NH4NO3 hay không.
Nếu phản ứng không tạo thành muối NH4NO3 thì:
![]()
Khi đó khối lượng muối thu được là:
![]()
Do đó quá trình phản ứng đã tạo ra muối NH4NO3.
Gọi số mol muối NH4NO3 là t thì số mol N O 3 - tạo muối với kim loại là (1,1 + 8t) mol. Khối lượng muối tạo thành:
![]()

Đáp án B.

Khối lượng muối nitrat kim loại = 30 + 0,1 x 8 x 62 + 0,1 x 3 x 62 = 98,2 gam
--> m NH4NO3 = 127 - 98,2 = 28,8 gam
--> n NH4NO3 = 28,8/80 = 0,36 mol
--> n HNO3 bị khử = 2n N2O + n NO + n NH4NO3 = 0,1 x 2 + 0,1 + 0,36 = 0,66 mol.

Chọn A
Giả sử sau phản ứng có x mol NH4NO3. Ta có:
Quá trình cho e:
Mg → Mg+2 +2e
Al → Al+3 +3e
Zn → Zn+2 +2e
Quá trình nhận e: N+5 → N+1 - 4e
N+5 → N+2 - 3e
N+5 → N-3 - 8e
DLBT e : 2nMg + 3nAl + 2nZn = 8nN2O + 3nNO + 8nNH4NO3
→ m muối = mKL + mNO3-(muối KL) + mNH4NO3
nNO3- (muối KL)= ne trao đổi
→157,05 = 31,25 + 62(8.0,1+3.0,1+8x) + 80x
x= 0,1 mol → nHNO3 đã bị khử = 2nN2O + nNO +nNH4NO3= 0,4 mol

Cho NaOH dư vào dung dịch X, đun nóng thu được 0,1 mol khí.
→Dung dịch X có chứa NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,1← 0, 1 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (1)
1,0 0,1 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
2,4← 0,2mol
Theo 2 bán phản ứng (1), (2):
nH+= 10nNH4++ 12.nN2= 10.0,1+ 12.0,2= 3,4 mol=nHNO3
→a= 3,4/2=1,7M
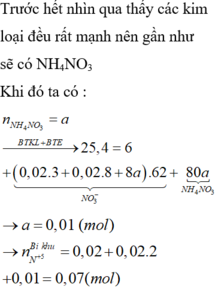
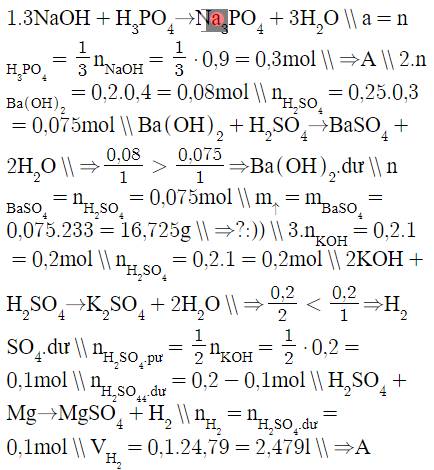

PTHH: 8Al + 30HNO3 --> 8Al(NO3)3 + 3N2O + 15H2O
____2,4 <---------------------------------0,9
=> nAl = 2,4 (mol)
\(QToxh:Al\rightarrow Al^{3+}+3e\\ QTkhử:2N^{+5}+8e\rightarrow N_2^{+1}\\ BTe:n_{Al}.3=n_{N_2O}.8\\ \Rightarrow n_{Al}=2,4\left(mol\right)\)