Ngâm 13g hỗn hợp gồm Zn và Cu trong dd CuSO4 dư. Phản ứng xong thu được chất rắn có khối lượng 12,84g. Thành phần % khối lượng của Cu trong hỗn hợp đầu là: A.98,77% B. 80% C.. 20% D. 1,23%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Phương trình phản ứng:
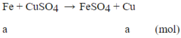
m tăng = (64-56).a = 1 ⇒a=0,125 mol
nFe = 0,125 ⇒nCu = (15-56.0,125)/64 = 0,125 mol
Thành phần phần trăm theo khối lượng:
⇒ % mCu = 53,33

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
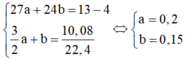
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.

\(PT:Fe+Cu3O_4\rightarrow FeSO_4+Cu\)
\(m\uparrow=-mFe+mCu=4\left(g\right)\)
\(nFe=\dfrac{4}{-56+64}=0,5\left(mol\right)\)
\(\Rightarrow mFe=28\left(g\right)\Rightarrow mCu=72\)

Đáp án D
Các phản ứng xảy ra:
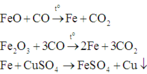
Hỗn hợp rắn thu được khi cho hỗn hợp phản ứng với dung dịch CuSO4 gồm Cu, FeO và Fe2O3.
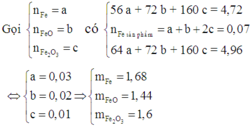

Đáp án A
Các phản ứng có thể xảy ra:
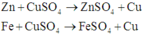
Trong 3 kim loại Zn, Fe và Cu thì Fe có khối lượng mol nhỏ nhất
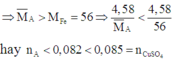
Do đó B chứa Cu2+ dư
Khi đó C chứa Cu trong A và Cu sinh ra sau phản ứng. Nên D chứa CuO.
B chứa Zn2+, Fe2+ và Cu2+ dư. Khi cho B tác dụng với dung dịch NaOH dư thì kết tủa thu được chứa Fe(OH)2 và Cu(OH)2 .
Do đó E chứa Fe2O3 và CuO.
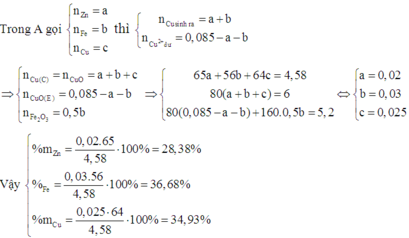

Đáp án A
Gọi nZn = a; nFe = b thì nCu = a + b
Vì khối lượng chất rắn trước và sau phản ứng bằng nhau nên mZn + mFe = mCu
Do đó 65a + 56b = 64(a+b) ⇔ a = 8b
Vậy phần trăm khối lượng cúa Zn trong hỗn hợp ban đầu là:
% m Z n = 65 . 8 b 65 . 8 b + 56 b . 100 % = 90 , 27 %
\(Zn+CuSO_4\to ZnSO_4+Cu\)
Đặt \(n_{Zn}=x(mol)\)
\(\Rightarrow m_{Zn(p/ứ)}-m_{Cu(p/ứ)}=65x-64x=13-12,84\\ \Rightarrow x=0,16(mol)\\ \Rightarrow \%_{Cu}=\dfrac{0,16.65}{13}.100\%=80\%\\ \Rightarrow B\)
Chọn B