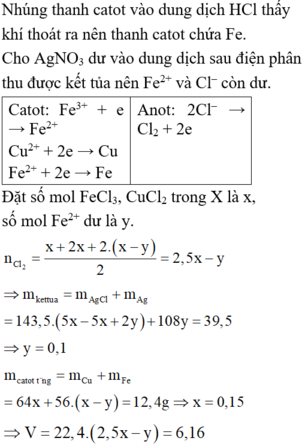Điện phần 500ml dung dịch CuCl2 tới khi lượng dung dịch giảm mất 27g thì nhừng điện phân. thổi khí H2S dư vào phần dung dịch còn lại sau khi điện phân, thu được 9,6g kết tủa.
Tính khối lượng catot tăng thêm. tính nồng độ mol của dung dịch trước khi điện phân. Tính điện lượng đã tiêu tốn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
CuSO4 + H2O → đ p d d Cu↓ + ½ O2↑ + H2SO4
Đặt nCuSO4 điện phân = x => mCu + mO2 = 8 64x + 32.0,5x = 8 => x = 0,1
CuSO4 dư + H2S → CuS↓ + H2SO4
=> nCuSO4 dư = nCuS = 0,1
Vậy nCuSO4 bđ = 0,2 => CM = 1M

Đáp án B
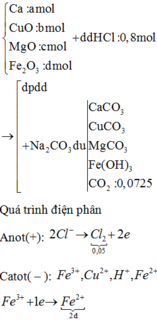
Thứ tự điện phân bên catot: Fe3+; Cu2+; Fe2+ và bên anot có Cl- bị điện phân.
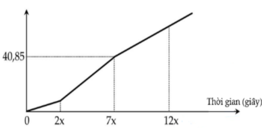
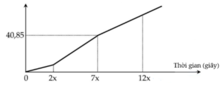
Nhìn vào đồ thị ta thấy có 3 đoạn dung dịch thay đổi.
+ Đoạn 1: bên catot chỉ có Fe3+ điện phân, anot có Cl-.
+ Đoạn 2: bên catot có Fe3+ và Cu2+, anot có Cl-.
+ Đoạn 3: bên catot có cả 3 ion điện phân, anot có Cl-.
Tại 2x (s):
Fe3+ + 1e → Fe2+ 2Cl- → Cl2 + 2e.
Gọi n(Cl-) = 2a → n(e) = n(Fe3+ bđ) = 2a mol.
→ Tại 7x (s) thì n(e) = 7a (mol
Fe3+ + 1e → Fe2+. 2Cl- → Cl2 + 2e.
2a→ 2a → 2a 7a ← 3,5a ← 7a
Cu2+ + 2e → Cu
→ n(e trong đp Cu2+) = 5a → n(Cu2+ bđ) = 2,5a (mol)
→ m(dd giảm) = m(Cu) + m(Cl2) = 64. 2,5a + 71. 3,5a = 40,85 → a = 0,1 mol
→ Tại 10x (s) thì n(e) = 1 mol.
Fe3+ + 1e → Fe2+. 2Cl- → Cl2 + 2e.
0,2→ 0,2 → 0,2 1 ← 0,5 ← 1
Cu2+ + 2e → Cu
0,25 → 0,5→ 0,25
Fe2+ + 2e → Fe.
→ n(e trong đp Fe2+) = 0,3 mol → n(Fe2+ đp) = 0,15 mol
Dung dịch sau phản ứng có Fe2+ dư và Cl-.
Kết tủa là Fe(OH)2 → n(Fe(OH)2) = 0,35 mol → n(Fe2+ dư) = n(Fe2+bđ) + 0,2 – 0,15 = 0,35
→ n(Fe2+ bđ) = 0,3 mol
Vậy hỗn hợp ban đầu có: FeCl3: 0,2 mol; CuCl2 0,25 mol và FeCl2 0,3 mol
Tại 12x (s): n(e) = 1,2 mol
Fe3+ + 1e → Fe2+. 2Cl- → Cl2 + 2e.
0,2→ 0,2 → 0,2 1,2 ← 0,6 ← 1,2
Cu2+ + 2e → Cu
0,25 → 0,5→ 0,25
Fe2+ + 2e → Fe
0,25← 0,5 → 0,25
Dung dịch sau điện phân có: Fe2+ (0,3 + 0,2 – 0,25 = 0,25 mol) và Cl‑(0,5 mol)
Khi cho vào AgNO3 thu được Ag (0,25 mol) và AgCl (0,5 mol)
→ m = 98,75 (g)

Câu 1:
nNaCl = 0,5mol
Khí ở anot là clo.
nCl2=4,48/22,4=0,2mol
PTHH: 2KCl + 2H2O → 2KOH + H2 + Cl2
=> nCl2(pư )= nKOH=0,4mol
=> Dư 0,1 mol KCl.
AgNO3+KCl→AgCl+H2O
2AgNO3+2KOH→Ag2O+2KNO3+H2O
=> m↓=mAgCl+mAg2O=0,1.143,5+0,2.232=60,75g
Câu 2:
Gọi x là mol CuCl2 phản ứng
PTHH: CuCl2 →Cu+Cl2
Khối lượng dd giảm là khối lượng Cu và khí clo.
=> 64x+71x=27
=> x=0,2
Khối lượng catot tăng là khối lượng Cu.
=> Δmcatot=0,2.64=12,8g
=> nCuS↓=9,6/96=0,1mol=nCuCl2dư
=> ΣnCuCl2=0,2+0,1=0,3mol
=> CMCuCl2=0,3/0,5=0,6M