Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi n là hoá trị của kim loại X
\(n_{H_2}=nn_X=\dfrac{10,8n}{X}\left(mol\right)\\ \Delta m_{dd}=10,8-2\cdot\dfrac{10,8n}{X}=9,6\\ n=\dfrac{1,2}{2.10,8}X=\dfrac{1}{18}X\)
X là kim loại mà X = 18n nên X là nguyên tố khí hiếm (vô lý)
Vậy không có kim loại X thoả đề

Đáp án C
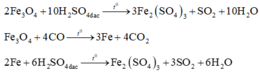
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.

Với lần thí nghiệm thứ nhất, có sự tham gia của O. Áp dụng định luật bảo toàn mol electron, ta có:
![]()
Với lần thí nghiệm thứ hai, không có sự tham gia của O. Áp dụng định luật bảo toàn mol
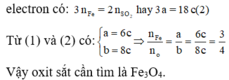

Đáp án C
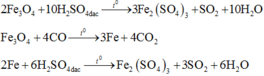
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.
Gọi thì ![]()
Các quá trình nhường và nhận electron diễn ra như sau:
Quá trình nhường electron:



Mức độ hoạt động hoá học của các kim loại theo chiều giảm dần :
X > Y > Z > T

Oxit A là oxit của kim loại M, hoá trị x. (x:nguyên, dương)
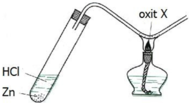
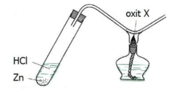
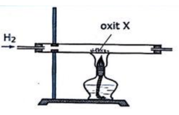
\(M_2O_x+xH_2\rightarrow\left(t^o\right)2M+xH_2O\left(1\right)\\ 2M+2xHCl\rightarrow2MCl_x+xH_2\left(2\right)\\ n_{H_2\left(1\right)}=n_{H_2O}=n_{O\left(mất\right)}=0,03\left(mol\right);n_{H_2\left(2\right)}=0,02\left(mol\right)\\ n_M=\dfrac{0,02.2}{x}=\dfrac{0,04}{x}\left(mol\right)\\ m_M=m_A-m_{O\left(mất\right)}=1,6-0,03.16=1,12\left(g\right)\\ \Rightarrow M_M=\dfrac{1,12}{\dfrac{0,04}{x}}=28x\left(\dfrac{g}{mol}\right)\)
Xét các TH: x=1;x=2;x=3 => Nhận TH x=2 khi đó MM=56(g/mol)
=>M là Sắt(Fe=56)
Đặt CTTQ A là : FeaOb (x,y:nguyên, dương)
\(a=\dfrac{1,12}{56}=0,02\left(mol\right);b=n_{O\left(mất\right)}=0,03\left(mol\right)\\ \Rightarrow a:b=0,02:0,03=2:3\\ \Rightarrow A:Fe_2O_3\)

Đáp án A
H2 chỉ khử được oxit của kim loại sau Al trong dãy hoạt động hóa học