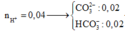Nhỏ từ từ từng giọt đến hết 40 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M. Sau khi phản ứng kết thúc, thể tích khí CO2 thu được ở đktc là:
A. 448 ml.
B. 672 ml.
C. 336 ml.
D. 224 ml.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
+ Bản chất phản ứng (1) xảy ra hoàn toàn sau đó đến (2):
( 1 ) H + + C O 3 2 - H C O 3 - ( 2 ) H + + H C O 3 - C O 2 ↑ + H 2 O ⇒ n C O 2 = n H + - n C O 3 2 -
+ Sử dụng công thức trên suy ra: n C O 2 = 0 , 01 ⇒ V C O 2 = 224 m l

Chọn đáp án D
Vì nNaHCO3 = nNa2CO3 ⇒ nHCO3– = nCO32–.
+ Đặt nHCO3– pứ = nCO32– pứ = a mol.
⇒ nHCO3– pứ × 1 + nCO32– pứ × 2 = nHCl ⇔ 3a = 0,03 a = 0,01
⇒ nCO2 = nHCO3– pứ + nCO32– pứ = a + a = 0,02 mol ⇒ Chọn D

nHCl = 0,03; nCO32- = 0,02; nHCO3- = 0,02
Khi cho từ từ axit vào muối cacbonat, phản ứng xảy ra theo thứ tự:
CO32- + H+ → HCO3- sau đó H+ dư + HCO3- → CO2 + H2O
0,02 → 0,02 → 0,02 (0,01) (0,02 + 0,02) → 0,01
Vậy nCO2 = 0,01 ⇒ Chọn C.

Chọn đáp án C
Nhỏ từ từ 0,03 mol HCl vào 0,02 mol Na2CO3 và 0,02 mol NaHCO3 thì trước tiên có phản ứng:
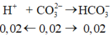 (1)
(1)
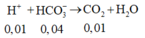 (2)
(2)
Từ (1) suy ra: .![]()
![]()
Từ (2) suy ra sau phản ứng (2)
H
C
O
-
3
dư, H+ hết nên ![]()
Đáp án A
Ta có: