Cho 8,0 gam hơi ancol đơn chức X qua CuO (lấy dư) nung nóng thu được 11,2 gam hỗn hợp chất lỏng gồm ancol, anđehit và nước. Vậy hiệu suất của phản ứng oxi hoá ancol là:
A. 70%.
B. 75%
C. 60%.
D. 80%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
● Cách 1: Tính toán theo phương trình phản ứng
Khối lượng hỗn hợp X tăng lên so với khối lượng ancol ban đầu là do lượng O trong CuO phản ứng đã chuyển vào H 2 O và CH 3 COOH .
Theo giả thiết, suy ra :
n H 2 = 0 , 0375 n CuO phản ứng = n O phản ứng
= (3,3 - 2,3):16 = 0,0625
Gọi số mol của ancol tham gia phản ứng là x, y và số mol ancol dư là z.
Phương trình phản ứng :
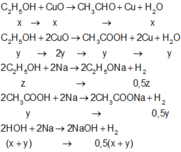
⇒ n C 2 H 5 OH bđ = x + y + z = 0 , 05 n H 2 = 0 , 5 y + 0 , 5 z + 0 , 5 x + 0 , 5 y = 0 , 0375 n CuO pư = x + 2 y = 0 , 0625 ⇒ x = 0 , 0125 ; y = 0 , 025 ; z = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %
● Cách 2: Sử dụng phương pháp bảo toàn nguyên tố
Sơ đồ phản ứng :
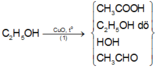
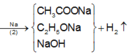
Bản chất phản ứng (1) là C 2 H 5 OH bị oxi hóa bởi CuO, khối lượng hỗn hợp sau phản ứng tăng lên là do O trong CuO chuyển vào H 2 O và CH 3 COOH . Ở phản ứng (2), CH 3 COOH , C 2 H 5 OH dư, HOH có nguyên tử H linh động trong nhóm –OH nên tham gia phản ứng thế Na giải phóng H 2 , CH 3 CHO không tham gia phản ứng này.
Sử dụng bảo toàn nguyên tố O trong phản ứng oxi hóa ancol và bảo toàn nguyên tố H của nhóm –OH trong phản ứng của X với Na, ta có :
n HOH = n CH 3 COOH = n O pư = 0 , 0625 n HOH + n CH 3 COOH + n C 2 H 5 OH dư = 2 n H 2 = 0 , 075 ⇒ n C 2 H 5 OH dư = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %

RCH2OH + CuO ![]() RCHO + Cu + H2O
RCHO + Cu + H2O
Ta có
mO trong CuO = 6,2 – 4,6 = 1,6 g
![]() nRCHO =nOtrong CuO= 1,6/16 = 0,1 mol
nRCHO =nOtrong CuO= 1,6/16 = 0,1 mol
Mặt khác, do ancol còn dư nên nancol bđ > 0,1 mol
![]()
![]()
![]() Ancol là CH3OH
Ancol là CH3OH
![]() RCHO là HCHO
RCHO là HCHO
HCHO ![]() 4Ag
4Ag
0,1 mol → 0,4 mol
![]() mAg = 108.0,4 = 43,2 g
mAg = 108.0,4 = 43,2 g
![]() Chọn C.
Chọn C.

Đáp án A
► T + NaOH dư/CaO → 1 ankan duy nhất
⇒ T gồm R(COOK)2 và H-RCOOK.
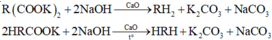
⇒ nT = nankan = 0,55 mol.
⇒ nanđehit = nX < 0,55 mol.
Nếu anđehit không phải là HCHO
⇒ nanđehit = nAg ÷ 2 = 1,2 mol ⇒ vô lí!.
► Anđehit là HCHO ⇒ X có dạng R(COOCH3)2 với số mol 0,3 mol
⇒ nY = 0,55 – 0,3 = 0,25 mol.
⇒ T gồm 0,3 mol R(COOK)2 và 0,25 mol HRCOOK với mT = 86,2(g)
⇒ R = 28 (C2H4).
⇒ %mX = 0,3 × 146 ÷ (0,3 × 146 + 0,25 × 74) × 100% = 70,3%

Đáp án C
BTKL ta có: mancol + mO(trong CuO) = mX
=> mO ( trong CuO) = 7,44 – 5,52 = 1,92 (g) => nO = 0,12 (mol)
ROH + [O]→ RCHO + H2O
Nếu ancol phản ứng hết thì nancol = nO (trong oxit) = 0,12 (mol) nhưng ancol dư sau phản ứng nên:
=> nROH > 0,12 (mol) => MROH < 5,52 :0,12 = 46 (g/mol)
=> ancol phải là CH3OH
=> andehit tương ứng là HCHO : 0,12 (mol)
=> nAg = 4nHCHO = 0,48 (mol) => mAg = 51,84 (g)
Chú ý:
nếu không chú ý sẽ nhầm lẫn ra được RCHO: 0,12 mol và tính ngay mAg = 25,92 g sẽ chọn ngay đáp án B mà không nghĩ trường hợp HCHO sẽ cho 4Ag => dẫn đến sai lầm

Đáp án A
Hướng dẫn RCH2OH + O → RCHO + H2O
Bảo toàn khối lượng: mancol + mO = manđehit => nO phản ứng = (6,2 – 4,6) / 16 = 0,1 mol
=> nRCH2OH phản ứng = 0,1 mol => nRCH2OH ban đầu > 0,1 mol
=> Mancol < 4,6 / 0,1 = 46 => ancol là CH3OH => anđehit tạo ra là HCHO
nAg = 4.nHCHO = 0,4 mol => mAg = 43,2 gam
Đáp án : D
Bảo toàn khối lượng : mancol + mO pứ = mhỗn hợp sau
=> nO pứ = 0,2 mol
RCH2OH + [O] -> RCHO + H2O
=> nancol pứ = nO pứ = 0,2 mol < nancol ban đầu
=> Mancol < 40g => ancol là CH3OH . nancol ban đầu = 0,25 mol
=> H% = 80%