Dung dịch X chứa a mol Ba(OH)2 và b mol NaOH. Sục khí CO2 dư vào dung dịch X, ta thấy lượng kết tủa biến đổi theo đồ thị: (các đơn vị được tính theo mol)
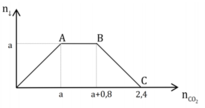
Giá trị a + b là
A. 0,8.
B. 1,0.
C. 1,6.
D. 1,8.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
Từ đồ thị ta thấy:
(1) Đoạn đi lên: Ba(OH)2 + CO2 → BaCO3↓ + H2O
(2) Đoạn ngang: 2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + CO2 + H2O → NaHCO3
(3) Đoạn đi xuống: BaCO3 + CO2 + H2O → Ba(HCO3)2
Xét (2) => nCO2 = nNaOH = 0,5 (mol) => m = 20 (g)
Tổng số mol CO2 phản ứng là 1,3 mol = nNaOH + 2nBa(OH)2
=> nBa(OH)2 = 0,4 mol = a
Vậy a = 0,4 và m = 20
Đáp án C

Chọn C
Dựa vào đồ thị :
(1) Đoạn đi lên : Ba(OH)2 + CO2 -> BaCO3 + H2O
(2) Đoạn ngang : 2NaOH + CO2 -> Na2CO3 + H2O
Na2CO3 + CO2 + H2O -> 2NaHCO3
(3) Đoạn đi xuống : BaCO3 + CO2 + H2O -> Ba(HCO3)2
Xét (2) => nCO2 = nNaOH = 0,5 mol => m = 20g
,Tổng số mol CO2 phản ứng là 1,3 mol = nNaOH + 2nBa(OH)2
=> nBa(OH)2 = 0,4 mol = a
=> a + m = 20,4

Đáp án B
Gọi số mol của Ba(OH)2 và NaOH lần lượt là a, b.
Nhận thấy tại 1,3 mol CO2 thì kết tủa bị hòa tan hoàn toàn
![]()
Tại (a + 0,5) mol CO2 thì kết tủa là a mol và lúc này xảy ra hiện tượng hòa tan kết tủa

Đáp án C
Ta có nOH– = 2a + m 40
Khi kết tủa tan hết thì chỉ có muối hidrocacbonat tức là lượng CO2 phản ứng cũng chính bằng số mol OH–.
⇒ 2a + m 40 = 1,3.
Khi lượng kết tủa bắt đầu giảm tức là CO2 đã phản ứng với OH– tạo a mol BaCO3 và còn lại là muối hirdocacbonat.
nCO2 = a + 0,5 = nBaCO3 + nNaHCO3 = a + m 40 ⇒ m = 20.
⇒ a = 0,4
Đáp án C
Cách 1:
Tại A: CO2 + 2OH− → CO2−3 + H2O
Ba2+ + CO2−3 → BaCO3↓
n B a C O 3 = a m o l
Quá trình A → B: CO2 + 2OH− → CO2−3 + H2O
CO2 + H2O + CO2−3 → 2HCO−3
Khối lượng kết tủa không đổi
Tại C:
a + b = 0,8 + 0,8 = 1,6
Cách 2: Phân tích đồ thị