Cho 200ml dung dịch H2SO4 0,5M vào dung dịch chứa a mol Na[Al(OH)4] được 7,8 gam kết tủa. Giá trị của a là
A. 0,025
B. 0,05
C. 0,1
D. 0,125
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nhận thấy nkết tủa = 0,02 mol < nNa[Al(OH)4] → Xảy ra 2 trường hợp,
Để thể tích dung dịch HCl là lớn nhất thì xảy ra quá trình hòa tan kết tủa
NaOH + HCl → NaCl + H2O
0,1 ----> 0,1
Na[Al(OH)4] + HCl → Al(OH)3 + H2O
0,02-----------> 0,02-------> 0,02
Na[Al(OH)4] + 4HCl → AlCl3 + 2H2O
0,03-------- ->0,12
Vậy nHCl = 0,1 + 0,02 + 0,12 = 0,24 mol → V= 0,12 lít.
Đáp án C

Đáp án C
Bản chất phản ứng là :
Lượng NaOH dùng nhiều nhất để tạo ra 0,1 mol Al OH 3 khi xảy ra cả phản ứng (3). Suy ra dung dịch sau phản ứng có chứa các ion SO 4 2 - , Na + , Al OH 4 -
Trong đó :
n SO 4 2 - = n H 2 SO 4 + 3 n Al 2 so 4 3 = 0 , 4 mol
n Al OH 4 - = n Al 3 + - n Al OH 3 = 2 n Al 2 ( SO 4 ) 3 - n Al OH 3 = 0 , 1 mol
Áp dụng bảo toàn điện tích cho dung dịch sau phản ứng, ta có :
n NaOH = n Na + = n Al OH 4 - + 2 n SO 4 2 - = 0 , 9 mol
⇒ V dd NaOH 2 M = 0 , 45 lit

Đáp án C
Ta có :
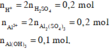
Dựa vào bản chất phản ứng và giả thiết, ta có đồ thị :

Dựa vào dạng hình học của đồ thị, ta thấy :
n Al ( OH ) 3 = 0 , 1 mol ⇒ n NaOH max = 0 , 9 mol ⇒ V dd NaOH 2 M = 0 , 9 2 = 0 , 45 lít
Đáp án D
• 0,1 mol H2SO4 + a mol Na[Al(OH)4] → 0,1 mol Al(OH)3↓
• H2SO4 + 2Na[Al(OH)4] →
Na2SO4 + 2Al(OH)3↓ + 2H2O (*)
3H2SO4 + 2Al(OH)3 → Al2(SO4)3 + 6H2O (**)
Theo (*) nH2SO4 = a/2 mol; nAl(OH)3 = a mol.
Theo (**) nAl(OH)3 phản ứng = a - 0,1 mol
→ nH2SO4 = 3/2 (a - 0,1) mol
→ ∑nH2SO4 = a/2 + 3/2 (a - 0,1) = 0,1
→ a = 0,125 mol