Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b = 3a và 7m = 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là:
A. C3H8
B. C2H6
C. C3H4O2
D. C3H6O2

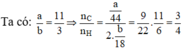
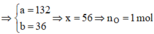






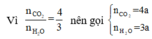
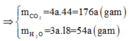
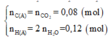
Đáp án C
Vì đốt cháy A thu được CO2 và H2O nên A chứa C, H, có thể có O.
Khi đó gọi công thức phân tử của A là CxHyOz
Nhận xét: Khi làm đến bước x : y = 3 :4 và kết hợp với quan sát 4 đáp án, ta có thể kết luận ngay A là C3H4O2.