Cho 200 ml dung dịch AgNO3 0,4M tác dụng với 300 ml dung dịch FeCl2 0,1M. Kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là:
A. 10,045
B. 10,77
C. 8,61
D. 11,85
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D.
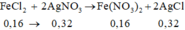
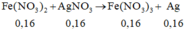
⇒ m = 143 , 5 . 0 , 32 + 108 . 0 , 16 = 63 , 2 gam

Đáp án A
Trong 300 ml dung dịch X có m gam Al 2 SO 4 3 , suy ra trong 150 ml dung dịch X sẽ có 0,5m gam Al 2 SO 4 3 và có số mol là x.
Lượng Al 2 SO 4 3 phản ứng ở 2 thí nghiệm là như nhau. Lượng OH - ở TN2 nhiều hơn ở TN1, lượng kết tủa (y mol) ở TN2 ít hơn ở TN1 (2y mol). Chứng tỏ ở TN2 kết tủa Al OH 3 đã bị hòa tan một phần, ở TN1 kết tủa có thể bị hòa tan hoặc chưa bị hòa tan.
● Nếu ở TN1 kết tủa Al OH 3 chưa bị hòa tan, áp dụng bảo toàn điện tích trong các dung dịch sau phản ứng, ta có :
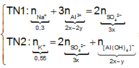
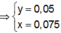
![]() thỏa mãn
thỏa mãn
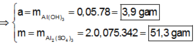
● Ở TN1 kết tủa Al OH 3 đã bị hòa tan, áp dụng bảo toàn điện tích cho dung dịch sau phản ứng, ta có:
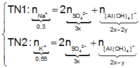
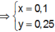
![]() (loại) (*)
(loại) (*)
PS : Nếu không sử dụng biểu thức (*) để biện luận loại trường hợp không thỏa mãn thì sẽ tính ra đáp án B. Nhưng đó là kết quả sai.

Đáp án : D
nH2 = 0,025 mol > nHCl = 0,02 mol
=> Kim loại M có thể tan trong nước tạo bazo
=> nCl = 0,02 mol ; nOH = 0,03 mol
=> Kết tủa gồm : 0,02 mol AgCl ; 0,015 mol Ag2O
=> m1 = 6,35g

Chọn đáp án B
Ta có


Chú ý : Đầu tiên Fe2+ sẽ (sinh ra khí NO) trước sau đó còn dư mới tác dụng với Ag+
m=0,6.143,5+0,05.108=91,5(g)
Đáp án là B. 10,77