Hòa tan hoàn toàn hỗn hợp rắn gồm Fe3O4 (1,2x mol) và Cu (x mol) vào dung dịch HCl (vừa đủ), kết thúc phản ứng chỉ thu được dung dịch X. Thêm dung dịch chứa 7,6 gam MgCl2 vào X, được dung dịch Y. Điện phân dung dịch Y đến khi nước bắt đầu điện phân ở anot thì ngừng điện phân, khi đó khối lượng dung dịch Y giảm 71,12 gam. Khối lượng muối khan thu được khi cô cạn dung dịch Y là:
A. 54,80 gam.
B. 60,64 gam.
C. 73,92 gam.
D. 68,24 gam.

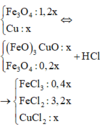
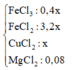


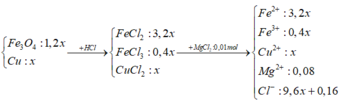



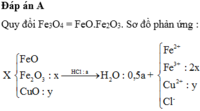
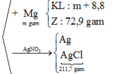
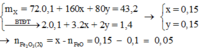
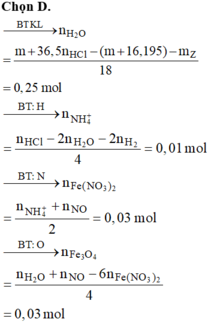

Quy đổi hỗn hợp ban đầu: ta có:
Thêm 0,08 mol MgCl2 ⇒ Ta có dung dịch Y gồm:
Sau khi điện phân đến khi anot có khí thoát ra ⇒ Có 3 kết tủa và 2 khí gồm:
Chú ý: phản ứng điện phân của MgCl2 và H2O.
MgCl2 + 2H2O Mg(OH)2↓ + Cl2↑ + H2↑
⇒ 3,6.56x + 64x + 0,08.58 + (4,8x + 0,08).71x + 0,08.2 = 71,12 x = 0,1.
⇒ mMuối/Y = 0,4×0,1×162,5 + 3,2×0,1×127 + 0,1×135 + 7,6 = 68,24 gam
Đáp án D