Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Fe3O4 + 8HCl -> FeCl2 + 2FeCl3 + 4H2O
1,4x -> 1,4x -> 2,8x
Cu + 2FeCl3 -> CuCl2 + 2FeCl2
x -> 2x
Y gồm : 0,06 mol MgCl2 ; x mol CuCl2 ; 3,4x mol FeCl2 ; 0,8x mol FeCl3
Điện phân đến khi anot xuất hiện khí :
Catot : 0,06 mol Mg2+ ; x mol Cu2+ ; 3,4x mol Fe2+ ; 0,8x mol Fe3+
Anot : (0,12 + 11,2x) mol Cl-
(Mg2+ không bị điện phân)
Vậy Catot : 2H2O + 2e -> H2 + 2OH-
Mol 0,12-> 0,06
mgiảm = mCu + mFe+ mH2 + mCl2
mmuối = mgiảm – mH2 + mMg (Vì bảo toàn e, số mol e H2 nhận đúng bằng số mol điện tích Mg2+ )
=> mmuối khan Y = 77,54 - 0,06.2 + 0,06.24 = 78,86g

Quy đổi hỗn hợp ban đầu: ta có:
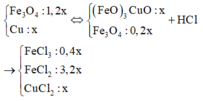
Thêm 0,08 mol MgCl2 ⇒ Ta có dung dịch Y gồm:
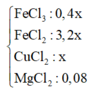
Sau khi điện phân đến khi anot có khí thoát ra ⇒ Có 3 kết tủa và 2 khí gồm:

Chú ý: phản ứng điện phân của MgCl2 và H2O.
MgCl2 + 2H2O Mg(OH)2↓ + Cl2↑ + H2↑
⇒ 3,6.56x + 64x + 0,08.58 + (4,8x + 0,08).71x + 0,08.2 = 71,12 x = 0,1.
⇒ mMuối/Y = 0,4×0,1×162,5 + 3,2×0,1×127 + 0,1×135 + 7,6 = 68,24 gam
Đáp án D

Đáp án D
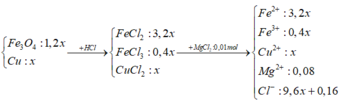
Điện phân dung dịch Y đến khi ở catot nước bắt đầu điện phân => Cl- điện phân hết

nOH- = 2nMg(OH)2 = 2.0,08 = 0,16 (mol)
Khối lượng dung dịch giảm :
∆ = m↓ + m↑ = mCu + mFe + mMg(OH)2 + mCl2 +mH2
<=> 71,12 = 64x + 56.3,6x + 0,08.58 + (9,6x + 0,08).35,5 + 0,04.2
=> x = 0,1 (mol)
mY = mkl + mCl-
= 64. 0,1 + 56.3,6.0,1 + 0,08.24 + (9,6.0,1 + 0,16).35,5
=68, 24(g)

Đáp án A
Đặt số mol của FeSO4, Cu(NO3)2, Cu lần lượt là x, y, z.
![]()
Trường hợp 1: NO 3 - phản ứng hết (x > 6y)
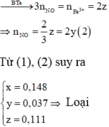
Trường hợp 2: Fe2+ phản ứng hết (x < 6y) => x = 2z (3)
Từ (1), (3) suy ra
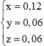
⇒ m muối = 56 . 0 , 12 + 64 ( 0 , 06 + 0 , 06 ) + 96 . 0 , 12 + 35 , 5 . 8 3 . 0 , 06 + 62 . 2 . 0 , 06 - 2 3 . 0 , 06 = 36 , 56 g

Đáp án D
nFe3+ = 0,08 (mol); H+ còn dư
Dd Y gồm: FeCl3 , FeCl2, CuCl2, HCl dư
Qúa trình điện phân dd Y
Catôt (Fe3+, Fe2+, Cu2+, H+) Anốt (Cl-)
Fe3+ +1e → Fe2+ 2Cl- + 2e → Cl2
0,08 → 0,08
Cu 2+ + 2e → Cu
x → 2x
2H+ + 2e → H2
Khi catốt có khí thì ngừng => chưa xảy ra phản ứng điện phân H+
Gọi nCuCl2 = x (mol)
=> ne trao đổi = 0,08 + 2x = 2nCl2
mdd giảm = mCu + mCl2 = 64x + 71( 0,04 + x) = 13,64
=> x = 0,08 (mol)
Gọi số mol Fe3O4 và Fe2O3 lần lượt là a và b mol
BTKL: 232a + 160b + 0,08.64 = 27,2 (1)
2Fe3+ + Cu → Fe2+ + Cu2+
=> nFe3+ sau = nFe3+ ban đầu – nCu
<=> 2a + 2b – 2.0,08 = 0,08 (2)
Từ (1) và (2) => a = 0,04 ; b = 0,08 mol
BTNT Fe: nFe2+ = nFe bđ – nFe3+ sau = 0,2 mol
nH+ dư = nHCl dư = nHCl bđ – 3nFeCl3 – 2nFeCl2 – 2nCuCl2 = 0,1 mol
Sau điện phân thì nFe2+ = 0,28 (mol); nCl- = 0,66 (mol); nH+ = 0,1 (mol)
Khi cho AgNO3 vào:
3Fe2+ + 4H+ + NO3- →3Fe3+ + NO + H2O
0,075← 0,1
Ag+ + Fe2+ → Fe3+ + Ag↓
(0,28 – 0,075)→ 0,205
Ag+ + Cl- → AgCl↓
0,66 → 0,66
m↓ = mAg + mAgCl = 0,205.108 + 0,66.143,5 = 116,85(g)

Quy hỗn hợp thành Fe2O3, FeO và CuO với số mol lần lượt là a b và c.
Ta có sơ đồ phản ứng:
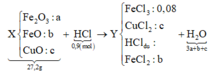
Khi điện phân dung dịch Y đến khi catot thoát khí ⇒ FeCl3 và CuCl2 đã bị điện phân hết.
⇒ mGiảm = nFeCl3×35,5 + nCuCl2×135 = 13,64 gam Û nCuCl2 = 0,08 mol.

●Tóm lại sau điện phân dung dịch chứa: nFeCl2 = 0,28 mol và nHCl = 0,1 mol.
Cho dung dịch sau điện phân + AgNO3 ⇒ 3Fe2+ + 4H+ + NO3– → Fe3+ + NO + 2H2O.
⇒ nFe2+ bị mất đi = 0,1 × 3 ÷ 4 = 0,075 mol
⇒ nFe2+ còn lại = 0,28 – 0,075 = 0,205 mol.
⇒ nAg = nFe2+ = 0,205 mol
nAgCl = nCl– = 0,28×2 + 0,1 = mol.
⇒ m↓ = mAg + mAgCl = 0,205×108 + 0,66×143,5 = 116,85
Đáp án A

nCuCO3 = nCO2 = 0,11 mol
nNa2SO3 = nSO2 = 0,14 mol
Thể tích dung dịch axit là x lít => nHCl = x và nH2SO4 = 0,5x => nH2O = x
BTKL:36,5x+98.0,5x+m=m+8,475+0,25.55,2+18x => x = 0,33
Dung dịch Y chứa SO42- (0,165), Cl- (0,33), Na+ (0,28) => nCu2+ = 0,19 => nCuO = 0,08
=> m = 37,68 và nFe = 0,0942
nCu2+ bị đp = 0,19.94% = 0,1786
=> n e trao đổi = nCl- + 4nO2 => nO2 = 0,068
=> nH+ = 4nO2 = 0,0272
Fe với dung dịch Z: nFe pư = nCu2+ + nH+/2 = 0,025
=> m1 = mFe dư + mCu = 4,6048 gam
Đáp án C

Đáp án C
nCuCO3 = nCO2 = 0,11 mol
nNa2SO3 = nSO2 = 0,14 mol
Thể tích dung dịch axit là x lít => nHCl = x và nH2SO4 = 0,5x => nH2O = x
BTKL: 36,5x+98.0,5x+m=m+8,475+0,25.55,2+18x => x = 0,33
Dung dịch Y chứa SO42- (0,165), Cl- (0,33), Na+ (0,28) ư
=> nCu2+ = 0,19 => nCuO = 0,08
=> m = 37,68 và nFe = 0,0942
nCu2+ bị đp = 0,19.94% = 0,1786
=> n e trao đổi = nCl- + 4nO2 => nO2 = 0,068
=> nH+ = 4nO2 = 0,0272
Fe với dung dịch Z: nFe pư = nCu2+ + nH+/2 = 0,025
=> m1 = mFe dư + mCu = 4,6048 gam
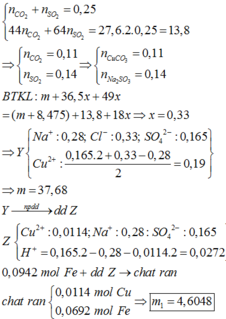
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
1,4x → 1,4x → 2,8x
Cu + 2FeCl3 → CuCl2 + 2FeCl2
x → 2x
Y gồm : 0,06 mol MgCl2 ; x mol CuCl2 ; 3,4x mol FeCl2 ; 0,8x mol FeCl3
Điện phân đến khi anot xuất hiện khí
Catot : 0,06 mol Mg2+ ; x mol Cu2+ ; 3,4x mol Fe2+ ; 0,8x mol Fe3+
Anot : (0,12 + 11,2x) mol Cl-
(Mg2+ không bị điện phân)
Vậy Catot : 2H2O + 2e → H2 + 2OH-
Mol 0,12→ 0,06
mgiảm = mCu + mFe+ mH2 + mCl2
mmuối = mgiảm – mH2 + mMg (Vì bảo toàn e, số mol e H2 nhận đúng bằng số mol điện tích Mg2+ )
=> mmuối khan Y = 77,54 - 0,06.2 + 0,06.24 = 78,86g
Đáp án C