Cho A, B, C là 3 nguyên tố thuộc ba chu kì liên tiếp trong bảng tuần hoàn và cùng thuộc một nhóm trong đó và . Tổng số proton của 3 nguyên tố đó là
A. 102
B. 58
C. 68
D. 82
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Vì số proton trong Y lớn hơn trong X 8 hạt. Nên dễ dàng tìm ra X là N (Z = 7) và Y là P (Z = 15).
A. Sai N không phản ứng với P.
B. Sai độ âm điện của N lớn hơn của P.
C. Đúng NH3 là phân tử phân cực.
D. Sai, oxi cao nhất của P là P2O5

Chọn đáp án C.
X và Y thuộc cùng một nhóm A và ở 2 chu kỳ liên tiếp, mặt khác ZX + ZY = 22 →X, Y thuộc chu kỳ nhỏ →ZY – ZX = 8 → ZX =7 (Nitơ) và ZY = 15 (Photpho).
A. Sai. Photpho không thể tác dụng với Nitơ.
B. Sai. Các nguyên tố thuộc cùng một nhóm theo chiều từ trên xuống dưới thì độ âm điện giảm dần → Độ âm điện của Y (Photpho) nhỏ hơn độ âm điện của X (Nitơ).
C. Đúng. Liên kết giữa H – N trong phân tử NH3 là liên kết cộng hóa trị có cực (phân cực về phía Nitơ) do chênh lệch độ âm điện giữa Nitơ và Hiđro.
D. Sai. Công thức oxit cao nhất của Y (Photpho) là P2O5 hay Y2O5

Tham Khảo:
A và B là hai nguyên tố ở cùng một phân nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn nên số thứ tự của chúng hơn kém nhau 8 hoặc 18 đơn vị (đúng bằng số nguyên tố trong một chu kỳ).
a,
Theo bài ra, tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32 nên (1).
Trường hợp 1:
A (Magie; chu kỳ 3, nhóm IIA); B: (Canxi; chu kỳ 4, nhóm IIA).
Trường hợp 2:
A (chu kỳ 2, nhóm VA); B: (chu kỳ 4, nhóm VIIB).
Trường hợp này A, B không cùng nhóm nên không thỏa mãn

A
A và B là hai nguyên tố ở cùng một phân nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn nên số thứ tự của chúng hơn kém nhau 8 hoặc 18 đơn vị (đúng bằng số nguyên tố trong một chu kỳ).
Theo bài ra, tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32 nên Z A + Z B = 32 .
● Trường hợp 1: Z B - Z A = 8 . Ta tìm được Z A = 12 ; Z B = 20 .
Cấu hình electron :
A : 1 s 2 2 s 2 2 p 6 3 s 2 (chu kỳ 3, nhóm IIA).
và B: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 (chu kỳ 4, nhóm IIA).
● Trường hợp 2: Z B - Z A = 18 . Ta tìm được Z A = 7 ; Z B = 25 .
Cấu hình electron :
A : 1 s 2 2 s 2 2 p 3 (chu kỳ 2, nhóm VA).
và B: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 2 (chu kỳ 4, nhóm VIIB).
Trường hợp này A, B không cùng nhóm nên không thỏa mãn.

B
X và Y là hai kim loại cùng nhóm A.
=> Y có nhiều hơn X là 8 hoặc 18 hoặc 32 electron.
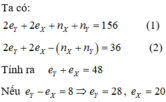
(không thuộc 2 chu kì)(loại).
![]()
Vậy 2 nguyên tố này là As và P, cùng thuộc nhóm VA và thuộc 2 chu kì (nhận).
![]()
(không thuộc 2 chu kì liên tiếp) (loại).
Vậy X là photpho (P).

Chọn C.
Vì số proton trong Y lớn hơn trong X 8 hạt nên ta tìm được X là N (Z = 7) và Y là P (Z= 15).
Đáp án A