Viết PTHH của các phản ứng của H 2 S với O 2 , S O 2 , nước clo. Trong các phản ứng đó H 2 S hể hiện tính khử hay tính oxi hoá, vì sao ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


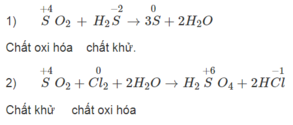
ở (1) SO 2 đóng vai trò là chất khử
ở (2) SO 2 đóng vai trò là chất oxi hóa.

Bàu 1
a) 4P+5O2--->2P2O5
S+O2--->SO2
3Fe+2O2--->Fe3O4
C2H4+3O2-->2CO2+2H2O
4Na+O2--->2Na2O
trừ phản ứng C2H4 thì tất cả đề là phản ứng hóa hợp
Bài 2
2H2+O2--->2H2O
2Mg+O2--->2MgO
2Cu+O2--->2CuO
S+O2--->SO2
4Al+3O2--->2Al2O3
C+O2---->CO2
4P+5O2--->2P2O5
Bài 1 :
a,
\(4P+5O_2\underrightarrow{^{to}}2P_2O_5\) (1)
\(S+O_2\underrightarrow{^{to}}SO_2\)(2)
\(3Fe+2O_2\underrightarrow{^{to}}Fe_3O_4\)(3)
\(C_2H_4+3O_2\underrightarrow{^{to}}2CO_2\uparrow+2H_2O\)(4)
\(4Na+O_2\underrightarrow{^{to}}2Na_2O\)(5)
\(2Ca+O_2\underrightarrow{^{to}}2CaO\)(6)
b, PHản ứng hóa hợp : (1) ; (2) ; (3) ;(5) ; (6)
Bài 2 :
\(2H_2+O_2\underrightarrow{^{to}}2H_2O\)
\(2Mg+O_2\underrightarrow{^{to}}2MgO\)
\(2Cu+O_2\underrightarrow{^{to}}2CuO\)
\(S+O_2\underrightarrow{^{to}}SO_2\)
\(4Al+3O_2\underrightarrow{^{to}}2Al_3O_3\)
\(C+O_2\underrightarrow{^{to}}CO_2\)
\(4P+5O_2\underrightarrow{^{to}}2P_2O_5\)

a) 2Mg + O2 \(\rightarrow\) 2MgO
Tỉ lệ :
2 : 1 : 2
b) 2H2 + O2 \(\rightarrow\) 2H2O
Tỉ lệ :
2 : 1 : 2
c) H2 + S \(\rightarrow\) H2S
Tỉ lệ :
1 : 1 : 1
d) 4K + O2 \(\rightarrow\) 2K2O
Tỉ lệ :
4 : 1 : 2
e) 2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Tỉ lệ :
2 : 6 : 2 : 3
g) 2Al(OH)3 \(\rightarrow\) Al2O3 + 3H2O
Tỉ lệ :
2 : 1 : 3
câu d mình chưa cân bằng nên sửa lại nha
a) 2Mg + O2 -> 2MgO
Tỉ lệ : 2 : 1 : 2
b) 2H2 + O2 -> 2H2O
Tỉ lệ : 2 : 1 : 2
c) S + H2 -> H2S
Tỉ lệ : 1 : 1 : 1
d) 4K + O2 -> 2K2O
Tỉ lệ : 4 : 1 : 2
e) 2Al + 6HCl -> 2AlCl3 + 3H2
Tỉ lệ : 2 : 6 : 2 : 3
g) 2Al(OH)3 ->t○ Al2O3 + 3H2O
Tỉ lệ : 2 : 1 : 3

1) \(C+O2-->CO2\)==>Pư hóa hợp
\(2Mg+O2-->2MgO\)==>Pư hóa hợp
\(4Al+3O2-->2Al2O3\)==>Pư hóa hợp
\(C2H6+\frac{7}{2}O2-->2CO2+3H2O\)
\(C2H2+\frac{5}{2}O2-->2CO2+H2O\)
2)
\(3Fe+2O2-->Fe3O4\)
\(S+O2-->SO2\)
\(CH4+2O2-->CO2+2H2O\)
\(2Cu+O2-->2CuO\)
\(4P+5O2-->2P2O5\)
\(C3H8O+\frac{9}{2}O2-->3CO2+4H2O\)
\(C4H10+\frac{13}{2}O2-->4CO2+5H2O\)
\(C7H16+11O2-->7CO2+8H2O\)

4H2 + O2 ---> 2H2O
2Mg + O2 ---> 2MgO
2Cu + O2 ---> 2CuO
S + O2 ---> SO2
4Al + 3O2 ---> 2Al2O3
C + O2 ---> CO2
4P + 5O2 ---> 2P2O5
- \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
- \(2Mg+O_2\underrightarrow{t^o}2MgO\)
- \(2Cu+O_2\underrightarrow{t^o}2CuO\)
- \(S+O_2\underrightarrow{t^o}SO_2\)
- \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
- \(C+O_2\underrightarrow{t^o}CO_2\)
- \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)

Đáp án : A
Có 8 chất phản ứng trừ dung dịch ZnCl2
Các trường hợp S bị oxi hóa lên +6 là : nước clo

1) \(4NH_3+5O_2\underrightarrow{t^o}4NO\uparrow+6H_2O\)
2) \(4NH_3+3O_2\underrightarrow{t^o}2N_2+6H_2O\)
3) \(2H_2S+O_2\underrightarrow{t^o}2S+2H_2O\)
4) \(6P+5KClO_3\underrightarrow{t^o}3P_2O_5+5KCl\)
5) \(3Fe_2O_3+CO\underrightarrow{t^o}2Fe_3O_4+CO_2\)

acâu 1
H2+ 1/2O2 --> H2O
Mg + 1/2O2 --> MgO
Cu+ 1/2O2-->CuO
S+O2 -->SO2
4Al+ 3O2-->2Al2O3
C+ O2--> CO2
2P+5/2O2--> P2O5
C2
a)
C+O2→CO2C+O2→CO2
nCO2=6,432=0,2nCO2=6,432=0,2
=>nCO2=nO2=0,2 mol
mCO2=0,2x44=8,8 g
b)
nC=612=0,5nC=612=0,5
nO2=19,232=0,6nO2=19,232=0,6
C+O2→CO2
TPU 0,5 0,6
PU 0,5-- 0,5-- 0,5
SPU 0--- 0,1--- 0,5
mCO2=0,5x44=22 g
CÂU 3
Đáp án:
CH4 + 2O2 → CO2 + 2H2O
2C2H2 + 5O2 → 4CO2 + 2H2O
C2H6O + 3O2 → 2CO2 + 3H2O
cái này là lớp 8 ( chương 4. Oxi và ko khí ) nha mn , e ấn nhầm
2 H 2 S + 3 O 2 → t ° 2S O 2 + 2 H 2 O
2 H 2 S + S O 2 → 3S + 2 H 2 O
H 2 S + 4 Cl 2 + 4 H 2 O → H 2 SO 4 + 8HCl
Trong các phản ứng trên, H 2 S thể hiện tính khử.