Bài 8: Cho hỗn hợp Na, K, Ba tác dụng hết với nước, thu được dung dịch X và 6,72l khí H 2 (đktc). Nếu cho X tác dụng hết với dung dịch A l N O 3 3 thì khối lượng kết tủa lớn nhất thu được là:
A. 7,8g
B. 15,6g
C. 46,8g
D. 3,9g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
• Na, K, Ba + H2O → 0,3 mol H2↑
Đặt công thức chung của ba kim loại là M
2 M + 2 n H 2 O → 2 M n + + 2 n O H - + n H 2 n O H - = 2 x 0 , 3 = 0 , 6 m o l
• X + Al(NO3)3 → ↓ lớn nhất

→ mAl(OH)3 = 0,2 × 78 = 15,6 gam

Đáp án C
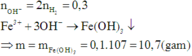
Nhận xét:Ở bài này, giả thiết cho thừa dữ kiện về tổng khối lượng hai kim loại. Đề bài sẽ hay hơn khi thay một trong hai kim loại kiềm trong hỗn hợp bằng kim loại Ba, khi đó kết tủa tạo thành gồm Fe(OH)3 và BaSO4. Để tính n F e ( O H ) 3 ta vẫn có cách làm như trên, tuy nhiên để tính được n B a S O 4 thì ta cần biết nBa , khi đó ta cần lập và giải hệ 2 phương trình bậc nhất 2 ẩn là nBa và nNa (hoặc nK ) theo giả thiết về khối lượng và n H 2 .

Đáp án B
nOH- = 2nH2 = 0,4
nCl- = 2nH2 = 0,3
m↓ = 5,2 + 0,3.17 = 10,3 g
mmuối = 5,2+0,3.35,5= 15,85 g

Quy đổi 2 kim loại kiềm Na và K là 1 kim loại trung bình . Khi đó:
2
M
¯
+
2
H
2
O
→
2
M
¯
O
H
H
2
1
6
M
¯
O
H
+
F
e
2
S
O
4
3
→
3
M
¯
2
S
O
4
+
2
F
e
O
H
3
(
2
)
Theo bài ta có: n H 2 = 3,36 22,4 = 0,15 m o l
⇒ n M ¯ O H = 2. n H 2 = 2.0,15 = 0,3 m o l ⇒ n F e ( O H ) 3 = 1 3 n M ¯ O H = 1 3 .0,3 = 0,1 m o l
⇒ m ↓ = m F e ( O H ) 3 = 0,1.107 = 10,7 g a m
⇒ Chọn C.
n O H - = 2 n H 2 = 2.6,72/22,4 = 0,6 mol
Cho X tác dụng với A l N O 3 3 , đạt kết tủa lớn nhất khi A l O H 3 tạo ra chưa bị hòa tan bởi các hidroxit kiềm, kiềm thổ trong X, khi đó:
A l 3 + + 3 O H - → A l O H 3
⇒ n A l O H 3 = 1/3 n O H - = 1/3 . 0,6 = 0,2 mol
⇒ m↓ = m A l O H 3 = 0,2.78 = 15,6g
⇒ Chọn B.