Đốt cháy hoàn toàn 3 gam chất A, thu được 2,24 lít CO2 (ở đktc) và 1,8 gam nước. Tỷ khối hơi của A so với metan là 3,75. Công thức cấu tạo của A biết A tác dụng được với NaHCO3 tạo khí là
A. HCOOCH3.
B. CH3COOH.
C. HCOOH.
D. C2H5COOH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Do đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,2\left(mol\right)\)
Xét mC + mH = 0,1.12 + 0,2.1 = 1,4 (g) < 4,6
=> A chứa C, H, O
\(n_O=\dfrac{4,6-1,4}{16}=0,2\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,2 = 1 : 2 : 2
=> CTPT: (CH2O2)n
Mà MA = 23.2 = 46 (g/mol)
=> n = 1
=> CTPT: CH2O2
CTCT: HCOOH

Chọn đáp án A.
Cả 4 đáp án X đều chứa 1N.
⇒ nX = 2nN2 = 0,2 mol.
⇒ Số C/X = 3; số H/X = 7
⇒ X là H2NCH2COOCH3

Chọn đáp án A
Cả 4 đáp án X đều chứa 1N ⇒ nX = 2nN2 = 0,2 mol.
⇒ số C/X = 3; số H/X = 7 ⇒ X là H2NCH2COOCH3 ⇒ chọn A.

Đáp án D
![]()
![]()
Có MA = 70. Lại có A tác dụng với H2 tạo thành ancol isobutylic => A là CH2=C(CH3)-CHO
Trong 0,35 mol chất A có nA = 0,005(mol)
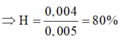
Ta thấy bài toán này cho rất thừa dữ kiện. Ta hoàn toàn không sử dụng đến dữ kiện về phản ứng đốt cháy. Để sử dụng dữ kiện của phản ứng đốt cháy ta có thể sửa lại đề bài như sau:
"Đốt cháy hoàn toàn 0,175 gam chất A chứa C, H, O thu được 0,224 lít CO2 (đktc). Cho 0,35 gam chất A tác dụng với H2 dư, xúc tác Ni thu được 0,296 gam rượu isobutylic. CTCT của A và hiệu suất phản ứng tạo thành rượu là?"
Khi đó ta sẽ tiến hành giải như sau:
Vì cho A tác dụng với H2 thu được rượu isobutylic =>A có 4 nguyên tử C trong phân tử
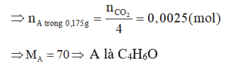
Đến đây ta tỉếp tục giải như trên.

a) MX = 146g/mol
VCO2 : VH2O = 6 : 5
=> nC : nH = 3 : 5
=> CTĐGN: (C3H5Oa)n
→ (41 + 16a).n = 146 → (a; n) = (4; 2) → X: C6H10O4
b) C6H10O4 + 6,5O2 → 6CO2 + 5H2O
0,05 0,325
=> p = 7,3g
c)
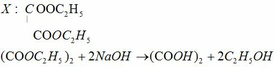

a) \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol)
Bảo toàn H: nH = 0,8 (mol)
Xét mC + mH = 0,4.12 + 0,8.1 = 5,6 (g)
=> A chứa C, H
Xét nC : nH = 0,4 : 0,8 = 1 : 2
=> CTPT: (CH2)n
Mà MA = 0,875.32 = 28 (g/mol)
=> n = 2
=> CTPT: C2H4
b) CTCT: \(CH_2=CH_2\)
c) A có làm mất màu dd Br2 do A có tác dụng với Br2
\(CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\)
Lời giải
nCO2 = 0,1 mol; nH2O = 0,1 mol
=> mC = 1,2 gam; mH = 0,2 gam
Bảo toàn khối lượng của axit: maxit = mC + mH + mO => mO = 1,6 gam
=> nC : nH : nO = 0,1 : 0,2 : 0,1 = 1 : 2 : 1 => CTPT có dạng CnH2nOn
MA = 3,75.16 = 60 => n = 2
=> CTPT: C2H4O2
Vì A tác dụng với NaHCO3 tạo khí => A là axit CH3COOH
Chọn B