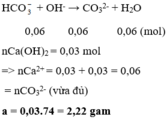
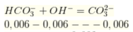Dung dịch A chứa : 0,15mol Ca2+ ; 0,6mol Cl- ; 0,1mol Mg2+ ; a mol HCO3- ; 0,4 mol Ba2+ . Cô cạn dung dịch A được chất rắn B . Nung B trong không khí đến khối lượng không đổi thu được m gam chất rắn khan . Giá trị m là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Dùng dung dịch K2CO3 để loại bỏ hết tất cả các ion ![]() ra khỏi dung dịch ban đầu:
ra khỏi dung dịch ban đầu:
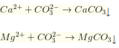
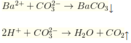

Có xuất hiện khí CO2 nên trong X chỉ chứa HCO3- (CO32- đã tạo hết thành HCO3-)
Cho Ca(OH)2 dư vào dung dịch X được 20gam kết tủa
Bảo toàn C ta có: ⇒ nHCO3-/X = nCaCO3 = 0,2 mol
Cho H+ vào dung dịch hỗn hợp muối CO32- và HCO3- nên có
H+ + CO32- → HCO3-
0,15 ← 0,15 → 0,15 mol
H+ còn lại sau pư = 0,2a – 0,15
n HCO3 = 0,15 + 0,1 = 0,25 mol
H+ + HCO3- → H2O + CO2
0,2a-0,15 → 0,2a-0,15 0,2a-0,15
nHCO3-/X = 0,25 – (0,2a – 0,15) = 0,4 – 0,2a
Cho Ca(OH)2 vào dung dịch X ta có: n CaCO3 = n HCO3-/X = 0,2 mol
⇒ 0,4 – 0,2a = 0,2 ⇒ a =1
⇒ b = (0,2a-0,15). 22,4 = 1,12l
Đáp án D.

Ta thấy Ag không tác dụng với C u S O 4 ⇒ Dd sau phản ứng có thể có các muối Z n S O 4 , F e S O 4 , C u S O 4
⇒ Chọn C.