Không tính thành phần phần trăm các nguyên tố, hãy sắp xếp các chất sau theo hàm lượng nitơ giảm dần. N2O5, NO2, N2O, N2O3, NO
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trong các hợp chất trên, số oxi hoá của nitơ lần lượt là: +2, +4, -3, -3, +1, +3, +5, -3.

C1:
%mCu(CuSO4)=\(\frac{64}{160}\).100%=40%
%mS(CuSO4)=\(\frac{32}{160}\).100%=20%
%mO(CuSO4)=100%-40%-20%=40%
%mC(CO2)=\(\frac{12}{44}\).100%=27,27%
%mO(CO2)=100%-27,27%=72,73%
%mC(CO)=\(\frac{12}{28}\).100%=42,86%
%mO(CO)=100%-42,86%=57,14%
C2:
%mN(N2O)=\(\frac{28}{44}\).100%=63,64% (1)
%mN(NO)=\(\frac{14}{30}\),100%=46,67% (2)
%mN(N2O3)=\(\frac{28}{76}\).100%=36,84% (3)
%mN(N2O5)=\(\frac{28}{108}\).100%=25,93% (4)
Từ (1),(2),(3)và(4) ta thấy hàm lượng Nitơ trong N2O cao nhất (63,64%)
C3:
Gọi CTHH của hợp chất A là FexOy
Ta có :
x : y = \(\frac{70\%}{56}\) : \(\frac{30\%}{16}\)
= 1,25 : 1,875
= 2 : 3
=> Fe2O3

Câu 2:
Trong 1 mol X: \(\left\{{}\begin{matrix}n_{Ag}=\dfrac{170.63,53\%}{108}=1\left(mol\right)\\n_N=\dfrac{170.8,23\%}{14}=1\left(mol\right)\\n_O=\dfrac{170\left(100\%-63,53\%-8,23\%\right)}{16}=3\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(AgNO_3\)
Câu 1:
\(a,\%_{Fe}=\dfrac{56}{180}\cdot100\%=31,11\%\\ \%_N=\dfrac{14\cdot2}{180}\cdot10\%=15,56\%\\ \%_O=100\%-31,11\%-15,56\%=53,33\%\\ b,\%_{N\left(N_2O\right)}=\dfrac{14\cdot2}{44}\cdot100\%=63,63\%\\ \%_{O\left(N_2O\right)}=100\%-63,63\%=36,37\%\\ \%_{N\left(NO\right)}=\dfrac{14}{30}\cdot100\%=46,67\%\\ \%_{O\left(NO\right)}=100\%-46,67\%=53,33\%\\ \%_{O\left(NO_2\right)}=\dfrac{16\cdot2}{46}\cdot100\%=69,57\%\\ \%_{N\left(NO_2\right)}=100\%-69,57\%=30,43\%\)

Về cách làm bạn xem lại GV hướng dẫn ở lớp, mình cho kết quả. Bạn check cho tiện nha!
a) C(II), N(III), Cl(I), Fe(III)
b) CO2 : C(IV), O(II)
NO: N(II), O(II)
NO2: N(IV), O(II)
N2O: N(I), O(II)
N2O5 : N(V), O(II)
NaCl: Na(I), Cl(I)
Al2O3: Al(III), O(II)
Fe(NO3)3: Fe(I), N(V), O(II), Fe(III)
H2SO4: H(I), S(VI), O(IV)
H3PO4: H(I), P(V), O(II)
Zn(OH)2: Zn(II), O(II), H(I)
Fe2(SO4)3: Fe(III), S(VI), O(II)
HCl: H(I), Cl(I)
Na2S: Na(I), S(II)
Ba(OH)2: Ba(II), O(II), H(I)
NaHCO3: Na(I), H(I), O(II), C(IV)
Na2SO4: Na(I), S(VI), O(II)
K3PO4: K(I), P(V), O(II)
Ca(HCO3)2: Ca(II), H(I), O(II), C(IV)
Mg(H2PO4)2: Mg(II), H(I), P(V), O(II)

Gọi hóa trị của N trong các hợp chất là x. Xét từng công thức hóa học:
- 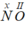 : Theo quy tắc hóa trị ta có: x.1 = II.1 ⇒ x = II
: Theo quy tắc hóa trị ta có: x.1 = II.1 ⇒ x = II
⇒ Hóa trị của N trong công thức NO là II
- 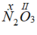 : Theo quy tắc hóa trị ta có: x.2 = II.3 ⇒ x = III
: Theo quy tắc hóa trị ta có: x.2 = II.3 ⇒ x = III
⇒ Hóa trị của N trong công thức N2O3 là III
- 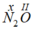 : Theo quy tắc hóa trị ta có: x.2 = II.1 ⇒ x = I
: Theo quy tắc hóa trị ta có: x.2 = II.1 ⇒ x = I
⇒ Hóa trị của N trong công thức N2O là I
- 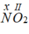 : Theo quy tắc hóa trị ta có x.1 = II.2 ⇒ x = 4
: Theo quy tắc hóa trị ta có x.1 = II.2 ⇒ x = 4
⇒ Hóa trị của N trong công thức NO2 là IV.

N trong NO có hóa trị II
N trong NO2 có hóa trị IV
N trong N2O có hóa trị I
N trong N2O5 có hóa trị V

a) FeO;Fe2O3;Fe3O4
- FeO có PTK=56+16=72
=> %O=\(\frac{16}{72}.100=22,2\%\)
- Fe2O3 cps PTK =56.2+16.3=160
=>%O=\(\frac{16.3}{160}.100=30\%\)
- Fe3O4 có PTK=56.3+16.4=232
=>%O=\(\frac{16.4}{232}.100=27,5\%\)
=>thành phần %oxi cao nhất là Fe2O3, thấp nhất là FeO
b)NO;NO2;N2O;N2O5
- NO có PTK=14+16=30
=> %O=\(\frac{16}{30}.100=53,3\%\)
- NO2 có PTK=14+16.2=46
=>%O=\(\frac{16.2}{46}.100=69,9\%\)
- N2O có PTK=14.2+16=44
=>%O=\(\frac{16}{44}.100=36,4\%\)
- NO2 có PTK=14.2+16.5=108
=>%O=\(\frac{16.5}{108}.100=74,1\%\)
thành phần %oxi cao nhất là N2O5, thấp nhất là N2O