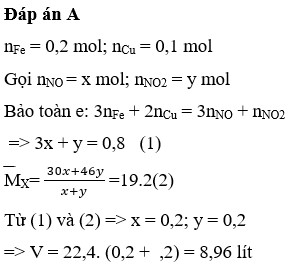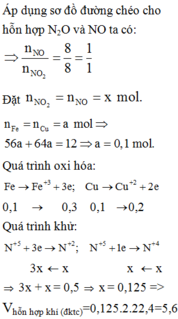23. Hoà tan hết 29,6g hỗn hợp gồm Cu và Fe ( tỉ lệ mol tương ứng là 2:3) vào dd HNO3 dư. Sau pư thu đc ddX và V hỗn hợp khí Y gồm NO2 và NO ( đktc). Biêta tỉ khối hơi của Y so vs H2 là 20,5. Gjas trị V là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Như vậy đề bài cho axit dư nên 2 muối thu được là Fe3+ và Cu2+
Gọi x là số mol Fe và Cu ta có: 56x + 64 x = 12 ⇒ x = 0,1 mol
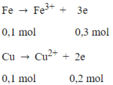
Mặt khác:
![]()
Đặt x, y là số mol của NO và NO2 thì 30x + 46 y = 38 (x+ y)
⇒ x = y
ne nhận = 3x + y = 4x, ne cho = 0,5 ⇒ 4x = 0,5 . Vậy x= 0,125 mol
V = 0,125.2. 22.4= 5,6 lít

Gọi số mol của Cu là a => nAl= 2a, nMg= 3a
mCu+mAl+mMg = 19 => a=0,1 =>nCu=0,1(mol);nAl=0,2(mol);nMg=0,3(mol)
dY/H2 =18,5 => M(Y)= 37 (dùng pp đường chéo) => nNO=nN2O
n(Y)= \(\dfrac{4,48}{22,4}\) =0,2 (mol)
Suy ra: nNO=nN2O= 0,1 (mol)
nNH4NO3 =\(\dfrac{\text{0,1.2+0,2.3+0,3.2−0,1.3−0,1.8 }}{8}\)=0,0375 (mol) bảo toàn e nhe
mm′ = mCu(NO3)2+ mAl(NO3)3 +mMg(NO3)2+mNH4NO3 = 108,8(g) ( khúc này bảo toàn nguyên tố Cu,Al,Mg => số mol của muối Cu2+,Al3+,Mg2+ )

Đáp án C
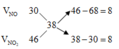
Áp dụng sơ đồ đường chéo cho hỗn hợp NO2 và NO ta có :
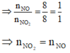
Đặt nFe = nCu = 0,1 mol.
Bảo toàn e
![]()
=> 0,1.3 + 0,1.2 = x + 3x => x = 0,125 mol
![]()

Đáp án C
Từ bài nFe=nCu=0,1
Sự oxi hóa
Sự khử
Fe0−3e→Fe+3
N+5+3e→N+2
0,1 0,3
3a a
Cu−2e→Cu+2
N+5+1e→N+4
0,1 0,2
b b
Bảo toàn e: 3a+b=0,5
Áp dụng phương pháp đường chéo với hỗn hợp khí ta được: a=b
Suy ra: a=b=0,125
V=5,6(l)

Đáp án C
Từ bài nFe = nCu = 0,1
Fe0 − 3e → Fe+3
0,1 0,3
N+5 + 3e → N+2
a 3a
Cu − 2e → Cu+2
0,1 0,2
N+5 + 1e → N+4
b b
Bảo toàn e: 3a + b = 0,5
Áp dụng phương pháp đường chéo với hỗn hợp khí ta được: a = b
Suy ra: a = b = 0,125
V = 5,6(l)