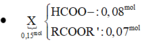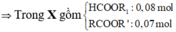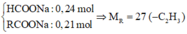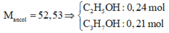Một hỗn hợp X gồm ancol etylic và phenol tác dụng với natri dư cho ra hỗn hợp 2 muối có tổng khối lượng là 25,2 gam. Cũng lượng hỗn hợp ấy tác dụng vừa đủ với 100ml dung dịch NaOH 1M. Tính số mol mỗi chất trong hỗn hợp X và thể tích hidro bay ra (đktc) trong phản ứng giữa X và Natri
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
nC6H5OH = nNaOH = 0,2 mol => mC6H5OH = 0,2.94 = 18,8 gam
=> mC2H5OH = 28,9 – 18,8 = 10,1 gam
=> %mC2H5OH = 10,1/28,9 = 34,95%

\(n_{H_2} = \dfrac{7,84}{22,4} = 0,35(mol) \\C_6H_5OH + KOH \to C_6H_5OK + H_2O\\ n_{C_6H_5OH} = n_{KOH} = 0,1.0,5 = 0,05(mol)\\ 2CH_3OH + 2Na \to 2CH_3ONa + H_2\\ 2C_6H_5OH + 2Na \to 2C_6H_5ONa + H_2\\ \)
Theo PTHH :
\(2n_{H_2} = n_{CH_3OH} + n_{C_6H_5OH}\\ \Rightarrow n_{CH_3OH} = 0,35.2 - 0,05 = 0,65(mol)\\ \%m_{CH_3OH} = \dfrac{0,65.32}{0,65.32 + 0,05.94}.100\% = 81,57\%\\ \%m_{C_6H_5OH} = 100\% - 81,57\% = 18,43\%\)

Chọn đáp án A
Este đơn chức chỉ có dạng HCOOR1 → + A g N O 3 / N H 3 2Ag↓ (dạng ankyl fomat).
Giả thiết: nAg = 0,16 mol → n H C O O R 1 = 0 , 08 m o l → este còn lại dạng R2COOR3 có 0,07 mol.
* Phản ứng: 41,7 gam X + NaOH → 36,06 gam hỗn hợp muối + 23,64 gam hỗn hợp ancol.
→ bảo toàn khối lượng có mNaOH = 18 gam → nNaOH = 0,45 mol.
Từ tỉ lệ hai este trong X → 41,7 gam X gồm 0,24 mol HCOOR1 và 0,21 mol R2COOR3.
→ 36,06 gam muối gồm 0,24 mol HCOONa và 0,21 mol R2COONa → R2 = 27 là gốc CH2=CH.
23,64 gam hỗn hợp ancol gồm 0,24 mol R1OH và 0,21 mol R3OH.
→ có phương trình nghiệm nguyên: 8R1 + 7R2 = 533 → R 2 = 29 → C 2 H 5 R 3 = 43 → C 3 H 7
Vậy, 41,7 gam X gồm 0,24 mol HCOOC2H5 và 0,21 mol C2H3COOC3H7.
→ %meste có phân tử khối nhỏ hơn trong X = 0,24 x 74 : 41,7 x 100% ≈ 42,59%

Chọn đáp án A
Vì nAg < 2nEste
⇒ X chứa 1 este có dạng HCOOR1
Ta có n H C O O R 1 = n A g ÷ 2 = 0 , 08 m o l
⇒ n R 2 C O O R 3 = 0 , 07 m o l
● Với phần 41,7 gam X bảo toàn khối lượng ta có
mNaOH pứ = 18 gam
⇔ nNaOH pứ = 0,45 mol
= 0,15 × 3.