Bài 10. Đốt cháy hoàn toàn m(g) hh kim loại Fe và Al cần dùng vừa đủ 5,6 lít khí O2 (đktc). Nếu lấy m(g) hh trên hòa tan hết trong dd HCl thì thấy thoát ra 10,08 lít khí H2 (đktc). Hãy tính m(g) hh kim loại và tính TP% mỗi kim loại trong hh đầu?
Bài 6. Khử hoàn toàn hh gồm CuO và Fe2O3 nặng 14g phải dùng hết 5,04 lít khí H2 (đktc). Viết các PTHH xảy ra và tính:
a) Thể tích H2 (đktc) đã dùng
b) Khối lượng hh kim loại thu được
c) Để có lượng khí H2 trên phải dùng bao nhiêu gam kim loại Zn và axit HCl
Bài 7. Khử hoàn toàn 19,7g hh gồm Fe3O4 và ZnO cần dùng vừa đủ 6,72 lít H2 (đktc) thu được hh kim loại. Tính:
a) Khối lượng mỗi oxit trong hh ban đầu?
b) Khối lượng mỗi kim loại thu được?
c) Để có lượng H2 trên phải dùng bao nhiêu gam kim loại Mg và axit H2SO4? Biết lượng axit dùng dư 10%

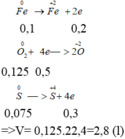
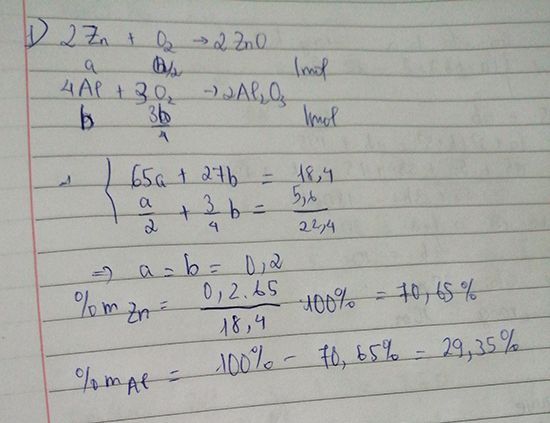
b6
nH2=V/22,4=5,04/22,4=0,225(mol)
Gọi a,b lần lượt là sô mol của Fe2O3 và CuO
pt1: Fe2O3 + 3H2-t0-> 2Fe +3H2O
cứ::1.................3..........2.............3 (mol)
vậy: a----------->3a------>2a (mol)
pt2: CuO +H2 -t0-> Cu +H2O
cứ:: 1...........1.............1........1 (mol)
vậy: b--------->b-------->b (mol)
từ 2pt và đề ta có:
160a+80b=14
3a+b=0,225
=> a=0,05(mol) ;b=0,075(mol)
=> mFe=n.M=0,05.56=2,8(g)
mCu=n.M=0,075.64=4,8(g)
=> mhh hai kim loại= mFe +mCu=2,8+4,8=7,6(g)
c) Pt3: Zn +2HCl -> ZnCl2 +H2
cứ::;; 1............2...........1..........1 (mol)
vậy: 0,225<---0,45<---0,225<--0,225(mol)
=> mZn=n.M=0,225.65=14,625(g)
mHCl=n.M=0,45.36,5=16,425(g)
b7
a) nH2:6,7222,4=0,3(mol)
Gọi x, y lần lượt là số mol của Fe3O4,ZnO
Fe3O4+4H2→3Fe+4H2O
1...................4............3............4(mol)
x..................4x.........3x...........4x(mol)
ZnO+H2→Zn+H2O
1..............1...........1.........1(mol)
y..............y............y.........y(mol)
Ta có:
{232x+81y=19,74
x+y=0,3
=>x=0,05
=>y=0.1
mFe3O4:232.0,05=11,6(g
mZnO:19,7−11,6=8,1(g)
b)mFe:56.0,15=8,4(g)
mZn:65.0,1=6,5(g)
c)Mg+H2SO4→MgSO4+H2
....1................1..................1............1(mol)
0,3................0,3................0,3.........0,3(mol)
mMg:0,3.24=7,2(g)mMg:0,3.24=7,2(g)
mH2SO4:0,3.98+0,3.98.10%=32.34(g)