Đốt cháy hoàn toàn 30 gam một hợp chất hữu cơ A thu được sản phẩm gồm 22,4 lít CO2 ở đktc và 18 gam nước.
a) Trong chất hữu cơ A có chứa những nguyên tố nào?
b) Biết khối lượng mol của hợp chất là 60 g/mol. Xác định công thức phân tử của chất A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, có nCO2=11/44=0,25 mol
có nC=nCO2=0,25mol=>mC=12.0,25=3(g)
có nH2O=6,75/18=0,375mol
có nH=2nH2O=2.0,375=0,75mol=>mH=0,75(g)
=>mH+mC=0,75+3=3,75=mA
=> A gồm nguyên tố C và H
b, gọi CTPT A là CxHy
có x/y=nC/nH=0,25/0,75=1/3
=> công thức thực nghiệm (CH3)n<=>CnH3n
có MA=30 gam/mol<=>12n+3n=30<=>n=2
vậy CTPT của A là C2H6
c;PTHH: CO2+2NaOH->Na2CO3+H2O
=> nNa2CO3=nCO2=0,25mol=>mNa2CO3=0,25.106=26,5 gam

Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{5,4}{18}=0,6\left(mol\right)\)
\(n_O=\dfrac{4,2-\left(0,3.12+0,6\right)}{16}=0\left(mol\right)\)
`->` A gồm C và H
Đặt CTTQ A: CxHy
\(x:y=0,3:0,6=1:2\)
CT có dạng: \(\left(CH_2\right)_n< 30\)
\(\Leftrightarrow n< 2,14\)
`@` Chỉ có `n=2` thỏa mãn
`->` CTPT A: \(C_2H_4\)
CTCT: \(CH_2=CH_2\) `->` A làm mất màu dd Brom
\(CH_2=CH_2+Br_{2\left(dd\right)}\rightarrow CH_2Br-CH_2Br\)

\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\) -> \(n_C=0,2\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\) -> \(n_H=0,4\)
\(m_C+m_H=0,2.12+0,4=2,8\left(g\right)\)
-> Trong A có \(m_O=6-2,8=3,2\left(g\right)\)
\(n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là \(C_xH_yO_z\)
\(x:y:z=n_C:n_H:n_O=0,2:0,4:0,2=1:2:1\)
\(\Leftrightarrow\left(CH_2O\right)_n=60.\Rightarrow n=2\)
a. CTPT của A là \(C_2H_4O_2\)
b. CTCT thu gọn:
\(CH_3COOH\)
mình không gõ được CTCT chi tiết (bạn lên mạng xem nhé)
c. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)

a.
Đốt cháy A thu được CO2 và H2O. Vậy A chứa nguyên tố C, H và có thể có O.
Ta có: \(n_C=\frac{6,6}{44}=0,15\left(mol\right),m_C=0,15.12=1,8\left(g\right)\)
\(n_{H_2O}=\frac{2,7}{18}=0,15\left(mol\right),m_H=0,15.2=0,3\left(g\right)\)
Khối lượng của Oxi : \(m_O=m_A-\left(m_H+m_C\right)=4,5-\left(1,8+0,3\right)=2,4g\)
Vậy A gồm có H, C và O.

a, - Đốt A thu CO2 và H2O
→ A chứa C và H, có thể có O.
Ta có:\(n_{CO_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\Rightarrow n_H=0,45.2=0,9\left(mol\right)\)
⇒ mC + mH = 0,45.12 + 0,9 = 6,3 (g)
→ A chứa C, H.
b, Gọi CTPT của A là CxHy.
⇒ x:y = 0,45: 0,9 = 1:2
→ CTPT của A có dạng là (CH2)n
Mà: \(M_A=28.1,5=42\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{42}{12+2}=3\)
Vậy: CTPT của A là C3H6.
c, Ta có: \(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
BTNT C, có: \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}\Rightarrow n_{Ca\left(HCO_3\right)_2}=0,075\left(mol\right)\)
BTNT Ca, có: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=0,375\left(mol\right)\)
\(\Rightarrow C_{M_{Ca\left(OH\right)_2}}=\dfrac{0,375}{0,4}=0,9375\left(M\right)\)

\(n_C=n_{CO_2}=0,15\left(mol\right)\\ n_H=2.n_{H_2O}=2.0,15=0,3\left(mol\right)\\ Ta.có:m_C+m_H=0,15.12+0,3.1=2,1\left(g\right)\\ A.tạo.bởi.2.NTHH:C,H\\ Đặt.CTTQ.A:C_aH_b\left(a,b:nguyên,dương\right)\\ a:b=n_C:n_H=0,15:0,3=1:2\\ \Rightarrow CTĐGN:\left(CH_2\right)_a\\ M_A=28\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow14a=28\\ \Leftrightarrow a=2\\ Vậy.A.là:C_2H_4\)

Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam) Trong A có 3 nguyên tố C,H,O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
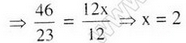
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O
Sơ đồ phản ứng:
\(A+O_2\rightarrow CO_2+H_2O\)
Dựa vào sản phẩm cháy, A chắc chắn chứa C và H, có thể chứa O.
Ta có:
\(n_{CO2}=n_{C.trong,A}=\frac{22,4}{22,4}=1\left(mol\right)\)
\(n_{H2O}=\frac{18}{18}=1\left(mol\right)\)
\(\Rightarrow n_{H.trong,A}=2n_{H2O}=2\left(mol\right)\)
\(\Rightarrow m_C+m_H=12.1+2.1=14\left(g\right)< 30\)
\(\Rightarrow m_O=30-14=16\left(g\right)\)
\(n_O=\frac{16}{16}=1\left(mol\right)\)
\(n_C:n_H:n_O=1:2:1\) nên A có dạng \(\left(CH_2O\right)_n\)
Vì \(M_A=60\Rightarrow30n=60\)
\(\Rightarrow n=2\)
Vậy A là C2H4O2
a) A chứa C, H, O
b) A là C2H4O2C2H4O2
Giải thích các bước giải:
Sơ đồ phản ứng:
A+O2→CO2+H2OA+O2→CO2+H2O
Dựa vào sản phẩm cháy, A chắc chắn chứa C và H, có thể chứa O.
Ta có:
nCO2=nC trong A=22,422,4=1 mol; nH2O=1818=1 mol→nH trong A=2nH2O=2 molnCO2=nC trong A=22,422,4=1 mol; nH2O=1818=1 mol→nH trong A=2nH2O=2 mol
→mC+mH=12.1+2.1=14 gam < 30→mO=30−14=16 gam→nO=1616=1 mol→mC+mH=12.1+2.1=14 gam < 30→mO=30−14=16 gam→nO=1616=1 mol
→nC:nH:nO=1:2:1→nC:nH:nO=1:2:1 nên A có dạng (CH2O)n(CH2O)n
Vì MA=60→30n=60→n=2MA=60→30n=60→n=2
Vậy A là C2H4O2
Nếu sai mong bạn bỏ qua.