Dẫn hỗn hợp gồm etan, eten, etin và butađien lần lượt đi qua bình 1 đựng dd AgNO3/dd NH3 dư, sau đó qua tiếp bình 2 đựng dd Br2 dư, thấy thoát ra khí X . Khí X thoát ra là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt :
nC2H4 = a (mol) , nC2H2 = b(mol)
nC2H6 = 4.48/22.4 = 0.2 (mol)
=> a + b = 0.5 - 0.2 = 0.3 (1)
m tằn = mC2H4 + mC2H2 = 8.1 (g)
=> 28a + 26b = 8.1 (2)
(1) , (2) :
a = 0.15
b = 0.15
%C2H2 = 0.15/0.5 * 100% = 30%

a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra khỏi bình là CH4 (metan).
b, Ta có: \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{1,12}{5,6}.100\%=20\%\\\%V_{C_2H_4}=100-20=80\%\end{matrix}\right.\)
c, Ta có: \(V_{C_2H_4}=5,6.80\%=4,48\left(l\right)\)
\(\Rightarrow n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,2.160=32\left(g\right)\)
Bạn tham khảo nhé!

Đáp án A
X gồm C4H4, C4H6, C4H8 và H2.
Đốt cháy hoàn toàn X cần 1,63 mol O2.
Nung X với Ni thu được hỗn hợp Y chỉ gồm các hidrocacbon.
Y gồm C4H4, C4H6, C4H8 và C4H10.
Dựa vào số mol O2 đốt cháy X cũng như Y giải được số mol C và H trong X lần lượt là 1,12 và 2,04
![]()
Khí thoát ra khỏi bình là C4H10 0,07 mol.
Khí phản ứng với dung dịch Br2 là C4H8 và C4H6 dạng CH2=CH-CH=CH2.
Khối lượng bình tăng là khối lượng của 2 hidrocacbon và số mol Br2 phản ứng là 0,11 mol.
Giải được số mol 2 hidrocacbon lần lượt là 0,07 và 0,02 mol.
Hidrocacbon tạo kết tủa với AgNO3/NH3 là C4H4 và C4H6 (but-1-in) có tổng số mol là 0,12 mol.
Mặt khác dựa vào bảo toàn H giải được số mol của 2 hidrocacbon này lần lượt là 0,03 và 0,09 mol.
Kết tủa gồm C4H3Ag 0,03 mol và C4H5Ag 0,09 mol, vậy m=19,26 gam

Đáp án D
15,48(g) C 4 H 4 C 4 H 8 C 4 H 6 H 2 → O 2 ( 1 , 63 ) C O 2 ( a ) H 2 O ( b )
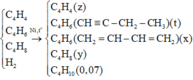
B T K L : 52 z + 54 t = 15 , 48 - 0 , 07 . 58 - 5 B T N T ( C ) : z + t = 1 , 12 - 0 , 07 . 4 - 0 , 02 . 4 - 0 , 07 . 4 4
→ x = 0 , 03 y = 0 , 09 → m = 0 , 03 . 159 + 0 , 09 . 161 = 19 , 26

Khí thoát ra là metan
\(\%V_{CH_4} = \dfrac{5,6}{13,44}.100\% =41,67\%\\ \%V_{C_2H_4} = 100\% - 41,67\% = 58,33\%\\ b) V_{C_2H_2} = 13,44 -5,6 = 7,84(lít)\\ n_{C_2H_2} = \dfrac{7,84}{22,4} = 0,35(mol)\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\\ n_{Br_2} = 2n_{C_2H_2} = 0,7(mol)\\ \Rightarrow C_{M_{Br_2}} = \dfrac{0,7}{0,25} = 2,8M\\ c)\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ V_{O_2} = 2V_{CH_4} + 3V_{C_2H_4} = 5,6.2 + 7,84.3 = 34,72(lít)\)

a)
C2H2 + 2AgNO3 + 2NH3 --> C2Ag2 + 2NH4NO3
C3H6 + Br2 --> C3H6Br2
b)
\(n_{C_2Ag_2}=\dfrac{3,6}{240}=0,015\left(mol\right)\)
=> nC2H2 = 0,015 (mol)
\(m_{tăng}=m_{C_3H_6}=2,1\left(g\right)\)
=> \(n_{C_3H_6}=\dfrac{2,1}{42}=0,05\left(mol\right)\)
\(n_{C_2H_6}=\dfrac{0,784}{22,4}=0,035\left(mol\right)\)
\(\left\{{}\begin{matrix}\%V_{C_2H_6}=\dfrac{0,035}{0,035+0,05+0,015}.100\%=35\%\\\%V_{C_3H_6}=\dfrac{0,05}{0,035+0,05+0,015}.100\%=50\%\\\%V_{C_2H_2}=\dfrac{0,015}{0,035+0,05+0,015}.100\%=15\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{C_2H_6}=\dfrac{0,035.30}{0,035.30+0,05.42+0,015.26}.100\%=29,661\%\\\%m_{C_3H_6}=\dfrac{0,05.42}{0,035.30+0,05.42+0,015.26}.100\%=59,322\%\\\%m_{C_2H_2}=\dfrac{0,015.26}{0,035.30+0,05.42+0,015.26}.100\%=11,017\%\end{matrix}\right.\)
c)
\(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
Bảo toàn C: \(n_{CaCO_3}+2.n_{Ca\left(HCO_3\right)_2}=0,25\left(mol\right)\)
=> \(n_{Ca\left(HCO_3\right)_2}=0,1\left(mol\right)\)
Bảo toàn Ca: \(n_{Ca\left(OH\right)_2}=0,15\left(mol\right)\)
=> \(V_{dd.Ca\left(OH\right)_2}=\dfrac{0,15}{1}=0,15\left(l\right)=150\left(ml\right)\)

a) \(n_{C_2Ag_2}=\dfrac{48}{240}=0,2\left(mol\right)\)
=> nC2H2 = 0,2 (mol)
\(n_{Br_2}=\dfrac{24}{160}=0,15\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,15<--0,15
\(n_{C_3H_8}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\left\{{}\begin{matrix}\%V_{C_3H_8}=\dfrac{0,15}{0,15+0,15+0,2}.100\%=30\%\\\%V_{C_2H_4}=\dfrac{0,15}{0,15+0,15+0,2}.100\%=30\%\\\%V_{C_2H_2}=\dfrac{0,2}{0,15+0,15+0,2}.100\%=40\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{C_3H_8}=\dfrac{0,15.44}{0,15.44+0,15.28+0,2.26}.100\%=41,25\%\\\%m_{C_2H_4}=\dfrac{0,15.28}{0,15.44+0,15.28+0,2.26}.100\%=26,25\%\\\%m_{C_2H_2}=\dfrac{0,2.26}{0,15.44+0,15.28+0,2.26}.100\%=32,5\%\end{matrix}\right.\)
b) Bảo toàn C; nCaCO3 = 1,15 (mol)
=> mCaCO3 = 1,15.100 = 115 (g)
c) \(n_{C_2H_2\left(bđ\right)}=\dfrac{0,2}{2}=0,1\left(mol\right)\)
=> nC2Ag2(lý thuyết) = 0,1 (mol)
\(H\%=\dfrac{19,2}{0,1.240}.100\%=80\%\)
https://hoc24.vn/cau-hoi/hon-hop-a-chua-etanpropenetincho-hon-hop-a-di-qua-dung-dich-chua-agno3nh3-dusau-phan-ung-thu-duoc-36-gam-ket-tua-vang-va-hon-hop-khi-bdan-toan-bo-b-qua-binh-dung-dung-dich-brom-duthay-khoi-luo.5464617579599
giúp mình câu này nữa mình tick cho

\(n_{ankan} = \dfrac{4,48}{22,4} = 0,2(mol)\\ \%V_{ankan} = \dfrac{0,2.22,4}{6,72}.100\% = 66,67\%\\ \%V_{anken} = 100\% -66,67\% = 33,33\%\\ \Rightarrow n_{anken} = \dfrac{6,72}{22,4}-0,2 = 0,1(mol)\\ Anken : C_nH_{2n}\\ m_{anken} = m_{tăng} = 5,6(gam)\\ \Rightarrow M_{anken} = 14n = \dfrac{5,6}{0,1} = 56 \Rightarrow n = 4\\ \text{CTPT của hai chất : } C_4H_{10} ; C_4H_8\)
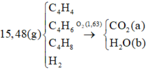
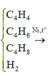
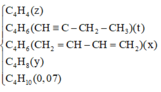
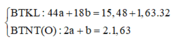
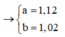
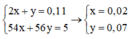
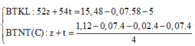
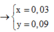
Khi cho hh vào AgNO3/NH3 thì C2H2 sẽ pứ tạo kết tủa vàng C2Ag2
Khi cho vào bình đựng dd Br2 thì C2H4 và C4H6 do có chứa liên kết π
Còn C2H6 sẽ không phản ứng với bất kì dd nào nên sẽ thoát ra (Khí)
Vậy đáp án là etan