X, Y là hai halogen thuộc hai chu kỳ liên tiếp nhau. Để làm kết tủa hết X và Y có trong 1,615g hỗn hợp NaX và NaY cần dùng 200 ml dung dịch AgNO3 0,1M. Xác định tên của X, Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Quy NaX và NaY về NaR
\(n_{AgNO_3}=0,15.0,2=0,05\left(mol\right)\)
PTHH: \(AgNO_3+NaR\rightarrow AgR\downarrow+NaNO_3\)
0,05------>0,05
\(\rightarrow M_R=\dfrac{2,2}{0,05}=44\left(g\text{/}mol\right)\)
Mà X và Y là 2 nguyên tố halogen thuộc 2 chu kì liên tiếp
\(\rightarrow M_X< M_R< M_Y\rightarrow M_X< 44< M_Y\)
---> X và Y là Cl và Br

NaX + AgNO 3 → NaNO 3 + AgX
a mol a mol a mol a mol
NaY + AgNO 3 → NaNO 3 + AgY
b mol b moi b mol b mol
n AgNO 3 = 0,2 x 150/1000 = 0,O3 mol
m AgNO 3 = 0,3 x 170 = 5,1g
n NaNO 3 = 0,O3 => m NaNO 3 = 0,03 x 85 = 2,55g
Áp dụng định luật bảo toàn khối lượng, ta có :
2,2 + 5,1 = 2,55 + m kết tủa → m kết tủa = 4,75 (gam)
(108 + X)a + (108 + Y)b = 4,75 ; a + b = 0,O3 (mol)
Xa + Yb + 15,1. Cho X > Y ; Xa + Xb > Xa + Yb > Ya + Yb
X > 1,51/0,03 > Y > X > 50,3 > Y
X và Y là các halogen liên tiếp, vậy đó là brom (80) và Cl (35,5).

a)
Gọi CTHH của hai muối là NaR
\(NaR +AgNO_3 \to AgR + NaNO_3\)
Ta có:
\(n_{NaR} = n_{AgNO_3} = 0,2.0,1 = 0,02(mol)\\ \Rightarrow 23 + R = \dfrac{1,615}{0,02} = 80,75\\ \Rightarrow R = 57,75\)
Vì MCl = 35,5 < R = 57,75 <MBr = 80 nên 2 muối là NaCl và NaBr
b)
\(\left\{{}\begin{matrix}NaCl:x\left(mol\right)\\NaBr:y\left(mol\right)\end{matrix}\right.\)→ \(\left\{{}\begin{matrix}58,5x+103y=1,615\\x+y=0,02\end{matrix}\right.\)→\(\left\{{}\begin{matrix}x=0,01\\y=0,01\end{matrix}\right.\)
Vậy :
\(\%m_{NaCl} = \dfrac{0,01.58,5}{1,615}.100\% = 36,22\%\\ \%m_{NaBr} = 100\% - 36,22\% = 63,78\%\)
c)
\(\left\{{}\begin{matrix}AgCl:x=0,01\left(mol\right)\\AgBr:y=0,01\left(mol\right)\end{matrix}\right.\)→ mkết tủa = 0,01.143,5 + 0,01.188=3,315(gam)
\(n_{AgNO_3}=0.2\cdot0.1=0.02\left(mol\right)\)
\(TH1:X:F\\ Y:Cl\)
\(NaCl+AgNO_3\rightarrow NâNO_3+AgCl\)
\(0.02........0.02............0.02..........0.02\)
\(m_{NaCl}=0.02\cdot58.5=1.17\left(g\right)< 1.615\left(g\right)\)
\(\%NaCl=\dfrac{1.17}{1.615}\cdot100\%=72.45\%\)
\(\%NaF=100-72.45=27.55\%\)
\(m_{AgCl}=0.02\cdot143.5=2.87\left(g\right)\)
\(TH2:Đặt:NaZ\)
\(NaZ+AgNO_3\rightarrow NaNO_3+AgZ\)
\(0.02.........0.02\)
\(M_{NaZ}=\dfrac{1.615}{0.02}=80.75\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow23+Z=80.75\\ \Rightarrow Z=57.75\)
\(X< Z< Y\Rightarrow X:Cl,Y:Br\)
\(Đặt:n_{NaCl}=a\left(mol\right),n_{NaBr}=b\left(mol\right)\)
\(\left\{{}\begin{matrix}a+b=0.02\\58.5a+103b=1.615\end{matrix}\right.\)
\(\Rightarrow a=b=0.01\)
\(\%NaCl=\dfrac{0.01\cdot58.5}{1.615}\cdot100\%=36.22\%\)
\(\%Nà=100-36.22=63.78\%\)
\(m_{\downarrow}=m_{AgCl}+m_{AgBr}=0.01\cdot143.5+0.01\cdot188=3.315\left(g\right)\)

Chọn A
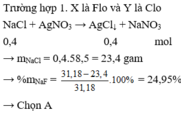
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Xét 2 trường hợp:
Trường hợp 1: Giả sử hai muối đều tạo kết tủa:
Gọi Z là halogen đại diện
\(NaZ+AgNO3\rightarrow AgZ+NaNO3\)
\(\dfrac{2,9825}{23+Z}\) \(\dfrac{0,7175}{108+Z}\)
\(\Rightarrow\dfrac{2,9825}{23+Z}=\dfrac{0,7175}{108+Z}\Leftrightarrow Z\approx2,4\) ( loại )
Trường hợp 2: Giả sử chỉ có một muối tạo kết tủa:
⇒ Đó là NaF và NaCl
NaF không phản ứng với AgNO3
NaCl + AgNO3 → AgCl + NaNO3
0,005 ← \(\dfrac{0,7175}{108+35,5}\)
mNaCl = 0,005 . ( 23 + 35,5 ) = 0,2925 (g) ( nhận )
Vậy hai nguyên tố X và Y cần tìm là: F và Cl

Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

Gọi CT chung của 2 muối là NaZ.
Ta có: \(n_{NaZ}=\dfrac{31,84}{23+M_Z}\left(mol\right)\)
\(n_{AgZ}=\dfrac{57,34}{108+M_Z}\left(mol\right)\)
BTNT Z, có: \(n_{NaZ}=n_{AgZ}\Rightarrow\dfrac{31,84}{23+M_Z}=\dfrac{57,34}{108+M_Z}\)
\(\Rightarrow M_Z\approx83,133\left(g/mol\right)\)
Mà: X, Y thuộc 2 chu kì kế tiếp của nhóm VIIA.
→ Br, I


Gọi CT chung của X và Y là \(\overline{X}\)
\(Na\overline{X}+AgNO_3\rightarrow NaNO_3+Ag\overline{X}\)
0,02_______0,02
\(\Rightarrow M_{Na\overline{X}}=23+\overline{X}=\frac{1,615}{0,02}\\ \Rightarrow\overline{X}=57,75\\ \Rightarrow Cl< \overline{X}< Br\)
Vậy 2 halogen là Cl và Br
á cảm ơn nhaaa mà
Cho 11,9 gam hỗn hợp Cu, Fe, Al vào dung dịch HCl dư. Sau phản ứng thấy có 4,48 lít khí sinh ra (đktc) và còn 6,4 gam chất rắn không tan. Tính khối lượng muối clorua khan thu được sau phản ứng.
giúp mình bài này vs dc hok , mai mình nộp rồi :(((