Cho 10,8 gam hỗn hợp X gồm Fe, Fe2O3 và oxit của kim loại hóa trị II tác dụng với 3,36 lít CO thu được khí Y và m(g) chất rắn Z. Dẫn toàn bộ lượng Y vào dung dịch nước vôi trong thu được 12,5 gam chất rắn không tan. Cho m(g) Z trên tác dụng vào dung dịch HCl dư thì thu được 2,24 lít khí và 0,05 mol chất rắn A không tan. Xác định công thức hóa học của oxit kim loại hóa trị II trên và tính thành phần phần trăm khối lượng mỗi chất trong hỗn hợp X? Biết các phản ứng xảy ra hoàn toàn, khí do ở dktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chuyển đổi hết từ khối lượng chất sang mol chất, rồi viết phương trình phản ứng , tính từng bước theo phương trình hóa học sẽ ra được.

Định hướng tư duy giải
Ta có:
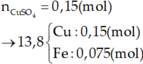
Dễ thấy 6 gam rắn là Fe2O3
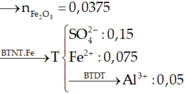
Có Al dư → Phần X phản ứng:
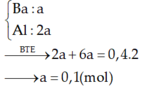
Chú ý: Vì chất tan thu được là Ba(AlO2)2→ tỷ lệ mol Ba : Al phải là 1 : 2
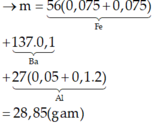

Đáp án D
Khi A tác dụng với CO thì: nO (pư) = nCO (pư) =0,125 mol
nNO = 0,09 mol, nHNO3 = 0,69 mol
Xét 2 trường hợp:
TH1: dung dịch C chứa Fe(NO3)3 + HNO3 (có thể dư)
Qui đổi hỗn hợp B thành Fe và O: F e : x m o l O : y m o l
Bảo toàn e ta có: 3x – 2y = 3nNO và 56x + 16y = 16,568 – 0,125.16 = 14,568
Giải hệ ⇒x = 0,2091 và y = 0,17865 mol ⇒ Số mol N sử dụng Fe(NO3)3: 0,2091 và NO: 0,09
Theo BTN: nN = 0,02091.3 + 0,09 = 0,7173 > 0,69 mol ⇒ loại
TH2: HNO3 hết, dung dịch C chứa 2 muối Fe(NO3)3 hoặc Fe(NO3)2
- Bảo toàn H: nH2O = 0,0345 mol
- Bảo toàn oxi cho toàn quá trình
y = (0,69 – 0,09).3 + 0,09.1 + 0,345 - 0,69.3 = 0,165 ⇔ 56x + 16y = 14,568 ⇔ x = 0,213 mol
Ta có:
→ a + b = 0,213
→ 3a+2b = 0,69 – 0,09 = 0,6
a =0,174; b=0,039
m = 0,174.107 + 0,039.90 = 22,128 gam

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lý => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol; y = 0,06 mol
=> rắn gồm 0,07 mol MgO và 0,03 mol F e 2 O 3 => m = 7,6 (g)

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư => C u 2 + hết
Giả sử chỉ có Mg phản ứng

Bảo toàn khối lượng gốc kim loại:
![]()
![]()
=> rắn gồm 0,07 mol MgO và 0,03 mol
![]()






\(n_{\frac{CO2}{Y}}=n_{CaCO3}=\frac{12,5}{100}=0,125\left(mol\right)\)
\(CO+\left[O\right]_{oxit.pư}\rightarrow CO_2\)
0,125__0,125_____0,125
\(\Rightarrow n_{CO_{pư}}< n_{CO_{bd}}\)
CO dư , oxit phản ứng hết
Nếu MO không phản ứng \(\Rightarrow Z\left\{{}\begin{matrix}Fe\\MO\end{matrix}\right.\) tan hết trong HCl (loại)
Vậy toàn bộ oxit trong X đã phản ứng hết
Xét \(X\left\{{}\begin{matrix}Fe\\M\end{matrix}\right.+\) HCl dư : Vì có rắn A không tan nên M phải là kim loại không tan trong HCl
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=n_{khí}=0,1\\n_M=0,05\end{matrix}\right.\)
Đặt \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Fe2O3}=b\left(mol\right)\\n_{MO}=c\left(mol\right)\end{matrix}\right.\)
Bảo toàn Fe : \(a+2b=0,1\)
Bảo toàn O : \(3b+c=0,125\)
\(c=0,05\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,025\\c=0,05\end{matrix}\right.\)
BTKL , \(m_X=m_{Fe}+m_{Fe2O3}+m_{CuO}\)
\(\Rightarrow m_{CuO}=10,8-0,05.56-0,025.160-0,05.80=4\left(g\right)\)
\(M=\frac{4}{0,05}-16=64\left(\frac{g}{mol}\right)\)
Vậy CTHH là CuO
\(\%m_{Fe}=\frac{0,05.56}{10,8}.100\%=25,93\%\)
\(\%m_{Fe2O3}=\frac{0,025.160}{10,8}=37,04\%\)
\(\%m_{CuO}=100\%-\left(25,93\%+37,04\%\right)=37,03\%\)