Cho 9 gam hỗn hợp Al, Mg tác dụng vừa đủ với hỗn hợp gồm 0,1 mol O2 và 0,25 mol
Cl2. Tính % khối lượng các kim loại trong hỗn hợp đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(n_{Mg} = a(mol) ; n_{Al} = b(mol)\\ \Rightarrow 24a + 27b = 5,7(1)\)
\(Mg^0 \to Mg^{+2} + 2e\\ Al^0 \to Al^{+3} + 3e\\ O_2 + 4e \to 2O^{-2}\\ Cl_2 + 2e \to 2Cl^-\)
Bảo toàn electron : \(2n_{Mg} + 3n_{Al} = 2a + 3b = 4n_{O_2} + 2n_{Cl_2} = 1,2(mol)\)(2)
Từ (1)(2) suy ra : a = -0,85< 0 ⇒ Sai đề
X{Mg, Al} + {Cl2, O2} → Z
Áp dụng định luật BTKL: mCl2 + mO2 = mZ – mX = 19,7 – 7,8 = 11,9 gam
Theo đề bài ta có hệ phương trình:
⎧⎪⎨⎪⎩nCl2+nO2=5,622,4=0,2571nCl2+32nO2=11,9→{nCl2=0,1nO2=0,15{nCl2+nO2=5,622,4=0,2571nCl2+32nO2=11,9→{nCl2=0,1nO2=0,15
Đặt số mol của Mg và Al lần lượt là x và y (mol)
- Khối lượng hỗn hợp: 24x + 27y = 7,8 (1)
- Bảo toàn e: 2nMg + 3nAl = 2nCl2 + 4nO2 => 2x + 3y = 0,1.2 + 0,15.4 hay 2x + 3y = 0,8 (2)
Giải (1) và (2) thu được x = 0,1 và y = 0,2
=> %mAl = 0,2.27/7,8 = 69,23%

Gọi số mol của Cu, Fe, Al trong 23,8 gam hhX lần lượt là x, y, z mol
→ mX = 64x + 56y + 27z = 23,8 (1)
\(n_{Cl_2}\) = x + 1,5y + 1,5z = 0,65 (2)
0,25 mol X + HCl → 0,2 mol H2 nên 0,2.(x + y + z) = 0,25.(y + 1,5z) (3)
Từ (1), (2), (3) => x = 0,2 mol; y = 0,1 mol; z = 0,2 mol
\(\%_{Cu} = \dfrac{0,2. 64}{23,8} \approx 53,78\%\)
\(\%_{Fe} = \dfrac{0,1 .56}{23,8} \approx 23,53\%\)
%Al ≈ 22,69%

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right),n_{Al}=c\left(mol\right)\)
\(m_X=64a+56b+27b=35.7\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{21.84}{22.4}=0.975\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{^{^{t^0}}}CuCl_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(Al+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}AlCl_3\)
\(n_{Cl_2}=a+1.5b+1.5c=0.975\left(mol\right)\left(2\right)\)
\(n_{hh}=ka+kb+kc=0.25\left(mol\right)\)
\(n_{H_2}=kb+k\cdot1.5c=0.2\left(mol\right)\)
\(\Leftrightarrow a-0.25b-0.875c=0\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=0.3,b=0.15,c=0.3\)
\(\%Cu=\dfrac{0.3\cdot64}{35.7}\cdot100\%=53.78\%\)
\(\%Fe=\dfrac{0.15\cdot56}{35.7}\cdot100\%=23.52\%\)
\(\text{%Al=22.7%}\)

Chọn C. Đặt nCl2=x mol và nO2=y mol. Phản ứng vừa đủ tạo muối gồm các ion sau: Al3+, Mg2+ , Cl- , O2-.
Theo định luât bảo toàn điện tích: 3nAl3+ +2nMg2+ = nCl- + 2nO2- = 2nCl2 + 4nO2
mmuối= 27nAl3+ +24nMg2+ + 35,5nCl- + 16nO2-
→ Hệ
3 . 0 , 2 + 2 . 0 , 1 = 2 x + 4 y 27 . 0 , 2 + 24 . 0 , 1 + 71 x + 32 y = 25 , 2 → x = 0 , 2 y = 0 , 1

- Từ giả thiết tính được : n Cl 2 = 0,035 mol; n O 2 = 0,025 mol
Theo ĐLBT khối lượng :
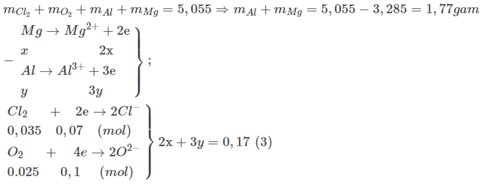
Từ (3)(4) ⇒ x = 0,04; y = 0,03
⇒ m Mg = 0,04.24 = 0,96g; m Al = 0,03.27 = 0,81g
Phản ứng không oxi hoá - khử

Đáp án : A
Trong 53,75g X có x mol Sn ; y mol Fe ; z mol Al
=> t(119x + 56y + 27z) = 53,75g
X + Cl2 -> SnCl4 ; FeCl3 ; AlCl3
⇒ t 4 x + 3 y + 3 z = 2 n C l 2 = 2 , 25 m o l
(Trong 0,4 mol lượng chất gấp t lần)
=> 9(119x + 56y + 27z) = 215(4x + 3y + 3z)
=> 211x – 141y – 402z = 0(1)
=> x + y + z = 0,4 mol(2)
n H 2 = x + y + 1,5z = 31/70 (mol) (3)
Từ (1,2,3) => z = 0,0857 mol
=> mAl = 2,314g

Đáp án A
+ S ơ đ ồ p h ả n ứ n g : C l 2 O 2 ⏟ 8 , 654 ( g ) + M g , A l Z n ⏟ 0 , 396 m o l → t 0 o x i t m u ố i ⏟ 23 , 246 ( g ) → V m l H C l 1 M M g 2 + , A l 3 + Z n 2 + , C l - ⏟ T → 0 , 572 m o l B a ( O H ) 2 M g ( O H ) 2 ↓ + P h ả n ứ n g c ủ a T v ớ i B a ( O H ) 2 : M g + 2 O H - → M g ( O H ) 2 Z n 2 + + 4 O H - → Z n O 2 2 - + 2 H 2 O A l 3 + + 4 O H - → A l O 2 - + 2 H 2 O + n M g = x n Z n = y n A l = z ⇒ n Y = x + y + z = 0 , 396 m Y = 24 x + 65 y + 27 z = 23 , 246 - 8 , 654 2 x + 4 y + 4 z = n O H - = 1 , 144 ⇒ x = 0 , 22 y = 0 , 12 z = 0 , 056 + m X = 71 n C l 2 + 32 n O 2 = 8 , 654 B T E : 2 n C l 2 + 4 n O 2 = 0 , 22 . 2 + 0 , 12 . 2 + 0 , 056 . 3 ⇒ n C l 2 = 0 , 034 n O 2 = 0 , 195 + n H + = 2 n O 2 - = 2 . 2 n O 2 = 0 , 78 m o l ⇒ V H C l 1 M = 0 , 78 l í t = 780 m l
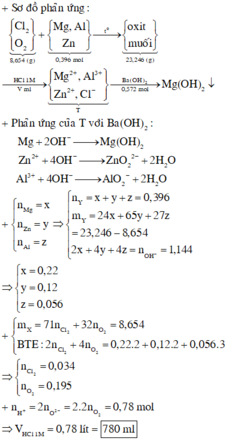

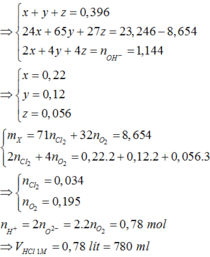
Gọi số mol Al, Mg lần lượt là: x, y (mol)
=> 27x + 24y = 9 (*)
Ta có: \(\overset{0}{Al}\rightarrow\overset{+3}{Al}+3e\)
x \(\rightarrow\) 3x (mol)
\(\overset{0}{Mg}\rightarrow\overset{+2}{Mg}+2e\)
y \(\rightarrow\) 2y (mol)
\(\overset{0}{O_2}+4e\rightarrow\overset{-2}{2O}\)
0,1\(\rightarrow\) 0,4 (mol)
\(\overset{0}{Cl_2}+2e\rightarrow\overset{-1}{2Cl}\)
0,25 \(\rightarrow\) 0,5 (mol)
Theo ĐLBT e, ta có: 3x +2y = 0,9 (**)
Từ (*) và (**), có: \(\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
=> mAl = 5,4 (g) => %mAl = 60%
=> %mMg = 40 %