Bài 1. Từ tinh dầu hoa nhài người ta tách ra được chất A. Phân tích thành phần phần trăm các nguyên tố cho kết quả như sau: 73,14% C, 7,32% H, còn lại là O. Biết khối lượng mol phân tử của chất A là 164 g/mol. Hãy xác định công thức phân tử của A.
Bài 2 Khí Oxi cần cho sự hô hấp của con người và động vật, cần để đổt nhiên liệu trong đời sống và sản xuất. Trong phòng thí nghiệm, khí Oxi được điều chế bằng cách đun nóng những hợp chất giàu Oxi và dễ bị phân hủy ở nhiệt độ cao.
Nếu phân hủy hoản toàn 73,5 (g) Kali clorat (KClo,) thu được Kali clorua (KCI) và khi Oxi.
a) Hãy lập phương trinh hóa học của phản ứng trên.
b) Tính khối lượng muối KCl thu được. c) Tính thể tích khí oxi sinh ra (đktc). d) Trong phòng thí nghiệm, để thu khí Oxi có thể sử dụng phương pháp đẩy không khí. Theo em phải đặt bình thu khí như thế nào là đúng trong hai cách như hình vẽ. Giải thích



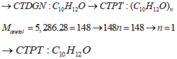
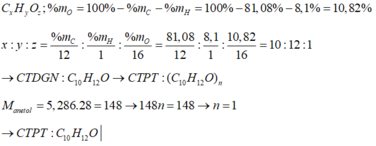
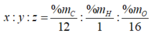
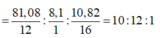

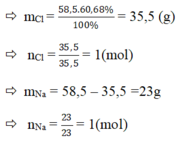
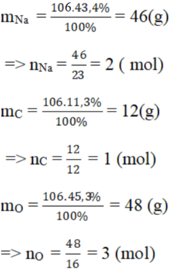
1.
Gọi công thức hóa học là \(C_xH_yO_z\)
\(x:y:z=\frac{\%_C}{12}:\frac{\%_H}{1}:\frac{\%_O}{16}\)
\(=\frac{73,14}{12}:\frac{7,32}{1}:\frac{19,54}{16}\)
\(=5:6:1\)
Vậy công thức đơn giản nhất là : \(C_5H_6O\)
Công thức nguyên là : \(\left(C_6H_6O\right)_n\)
Mà : \(M_A=164\rightarrow82n=164\Leftrightarrow n=2\rightarrow C_{10}H_{12}O_2\)
2.
a. \(2KClO_3\rightarrow2KCl+3O_2\)
b.\(n_{KCl}=\frac{73,5}{122,5}=0,5\left(mol\right)\)
Theo pthh :\(n_{KCl}=n_{KClO3}=0,6\left(mol\right)\)
\(\rightarrow m_{KCL}=0,6.74,5=44,7\left(g\right)\)
\(n_{O2}=\frac{3}{2}nKClO3=0,6.\frac{3}{2}=0,9\left(mol\right)\)
\(\rightarrow V_{O2}=0,9.22,4=20,16\left(l\right)\)
c.Do O2 nặng hơn không khí nên O2 sẽ chìm xuống dưới và không khí sẽ bị đẩy lên trên ( 32> 29) với 29 là M của không khí