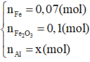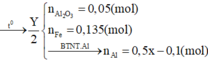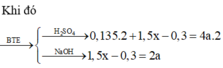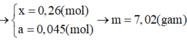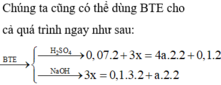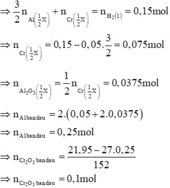Câu1:cho hỗn hợp A dạng bột gồm Al và Fe3O4.Nung A ở nhiệt độ cao để phản ứng nhiệt nhôm xảy ra hoàn toàn , thu được hỗn hợp B. Trộn đều B và chia B thành 2 phần không bằng nhau.
Phần 1 : cho tác dụng với Na OH dư thu được 1,176 lít khí (đktc) và chất không tan.Tách riêng chất không tan và đem hòa tan trong dung dịch HCl dư thu được 6,552 lít khí(đktc)
Phần 2 : Cho tác dụng với HCl dư thì thu được 6,552 lít khí (đktc).
Tính khối lượng hỗn hợp A và thành phần % các chất trong A
Câu2 :Dùng 0,3 mol H2 khử vừa đủ 16 gam 1 oxit kim loại có công thức M2On, lượng kim loại tạo thành cho tác dụng hết với dung dịch HCl dư tạo thành muối MCln và 0,2 mol H2.Xác định CTHH của oxit kim loại
Câu3:Cho 1 luồng khí CO dư đi qua m gam hỗn hợp A gồm CuO và Fe3O4 nung nóng , thu được chất rắn B và hỗn hợp khí D . Cho D đi qua dung dịch nước vôi trong thì thấy xuất hiện p gam kết tủa nữa. Giả thiết các phản ứng xảy ra hoàn toàn.
a)Viết phương trình phản ứng và xác định các chất trong B và D
b)Tính khối lượng chất rắn B theo m và p
c) Cho B tác dụng với dung dịch AgNO3 đến khi phản ứng hoàn toàn thu được chất rắn E gồm 2 kim loại và dung dịch Z
.Xác định các chất trong E và Z, viết các phương trình hóa học xảy ra.