Chia 31,2g Al(OH)3 làm 2 phần bằng nhau
a. Phần 1 cho tác dụng với 600ml dd HCl 1,5M. Tính khối lượng muối tạo thành
b. Phần 2 cho tác dụng với 50ml dd NaOH 2M. Tính khối lượng muối tạo thành
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2SO_4}=0,05\cdot3=0,15mol\)
a) \(H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2HCl\)
0,15 0,15 0,15 0,3
\(m_{ctBaCl_2}=0,15\cdot208=31,5\left(g\right)\)
\(m_{BaCl_2thamgia}=\dfrac{31,5}{20\%}\cdot100\%=157,5\left(g\right)\)
b) \(m_{BaSO_4}=0,15\cdot233=34,95\left(g\right)\)
c) \(Ca\left(OH\right)_2+H_2SO_4\rightarrow CaSO_4+2H_2O\)
0,15 0,15
\(m_{ctCa\left(OH\right)_2}=0,15\cdot74=11,1\left(g\right)\)
\(m_{ddCa\left(OH\right)_2}=\dfrac{11,1}{25\%}\cdot100\%=44,4\left(g\right)\)
\(\Rightarrow V_{Ca\left(OH\right)_2}=\dfrac{44,4}{1,15}=38,6\left(ml\right)\)

2Al+6HCl→2AlCl3+3H2
Zn+2HCl→ZnCl2+H2
2Al+6H2SO4→Al2(SO4)3+3SO2+6H2O
Zn+2H2SO4→ZnSO4+SO2+2H2O
Cu+2H2SO4→CuSO4+SO2+2H2O
nH2=0,3mol
nCu=0,15mol
Gọi a và b lần lượt là số mol của Al và Zn
27a+65b=17,25
3\2a+b=0,3
=> a=0,03, b=0,25
→nAl=0,03mol→mAl=1,62g
→nZn=0,25mol→mZn=32,5g
b)nHCl=3nAl+2nZn=0,59mol
→VHCl=0,592=0,295 l
c)
nAl2(SO4)3=1\2nAl=0,015mol
→mAl2(SO4)3=5,13g
nZnSO4=nZn=0,25mol
→mZnSO4=40,25g
nCuSO4=nCu=0,15mol
→mCuSO4=24g

nH2SO4= 2.0,05=0,1(mol)
PTHH: 2 NaOH + H2SO4 -> Na2SO4 + 2 H2O
a) nNaOH= 0,1.2=0,2(mol) => mNaOH=0,2.40=8(g)
=>mddNaOH= 8/20%= 40(g)
b) nNa2SO4=nH2SO4=0,1(mol)
=> mNa2SO4=142.0,1=14,2(g)

a) \(n_{HCl}=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
1 2 1 1 (mol)
0,2 0,4 0,2 0,2 (mol)
b) Thể tích khí hidro:
V = n.22,4 = 0,2.22,4 = 4,48 (l)
c) Khối lượng muối tạo thành:
\(m_{ZnCl_2}=n.M=0,2.\left(65+35,5.2\right)=27,2\left(g\right)\)
d) \(m_{ctHCl}=n.M=0,4.\left(1+35,5\right)=14,6\left(g\right)\)
\(C\%_{HCl}=\dfrac{m_{ctHCl}}{m_{ddHCl}}.100\%=\dfrac{14,6}{200}.100\%=7,3\%\)

\(a.HCl+NaOH\rightarrow NaCl+H_2O\)
PỨ trung hoà
\(b,n_{NaOH}=0,1.1=0,1mol\\ n_{NaCl}=n_{NaOH}=n_{HCl}0,1mol\\ m=m_{HCl}=0,1.36,5=3,65g\\ c,m_{NaCl}=0,1.58,5=5,85g\\ d,n_{HCl}=\dfrac{73.10}{100.36,5}=0,2mol\\ \Rightarrow\dfrac{0,1}{1}< \dfrac{0,2}{1}\Rightarrow HCl.dư\\ n_{HCl,pứ}=n_{NaOH}=0,1mol\\ m_{HCl,dư}=\left(0,2-0,1\right).36,5=3,65g\)

Đáp án C:
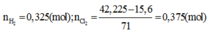
Tác dụng vói HCl: Cr, Zn, Ni tạo muối (II).
Ta gọi R là công thức chung của 2 kim loại Zn và Ni
Gọi x, y, z lần lượt là số mol của R, Al và Cr.
Bảo toàn electron ta có: ne cho= ne nhận
![]()
Tác dụng với Cl2 Zn và Ni tạo muối (II)
Bảo toàn electron ta có: necho = ne nhận
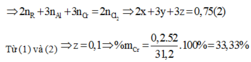

\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
a) Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
0,1 0,2 0,1
b) \(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(C_{ddHCl}=\dfrac{7,3.100}{200}=3,65\)0/0
c) \(n_{CuCl2}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
⇒ \(m_{CuCl2}=0,1.135=13,5\left(g\right)\)
Chúc bạn học tốt

a) \(NaOH+HCl\rightarrow NaCl+H_2O\)
0,1................0,3
LẬp tỉ lệ : \(\dfrac{0,1}{1}< \dfrac{0,3}{1}\)=> Sau pứ HCl dư
\(m_{NaCl}=0,1.58,5=5,85\left(g\right)\)
b) \(CM_{NaCl}=\dfrac{0,1}{0,2+0,3}=0,2M\)
\(CM_{HCl\left(dư\right)}=\dfrac{\left(0,3-0,1\right)}{0,2+0,3}=0,4M\)
b) n\(_{Al\left(OH\right)3}=0,2\left(mol\right)\)
Al(OH)3 + NaOH--->NaAlO2 +2H2O
Ta có
n\(_{NaOH}=0,05.2=0,1\left(mol\right)\)
=> Al(OH)3 dư
Theo pthh
n\(_{NaAlO2}=n_{NaOH}=0,1\left(mol\right)\)
m\(_{NaAlO2}=82.0,1=8,2\left(g\right)\)