1,Cho 100g NaCl 5,85%;H2SO4 49%;NaOH 20%;Ba2SO4 40%. Tính kl chất tan của từng chất trên
2,Cho 2,3g Na vào 100g nước thu đc dd NaOH có nồng độ bn % ?
3,Cho 100 g nước tác dụng với 2g Ca thu đc CaOH2 bn %?
4,Cho 100g nước tác dụng với Ca thu đc CaOH2 và 1,12ml H2 . Tính nồng độ % của CaOH2
5,Cho 8,8g FeS tác dụng với 100 g đ HCL thu đc FeCl2 có nồng độ bn %
6,Cho 100 g H2O tác dụng với K thu đc 2,24l khí H2 và dd KOH có nồng đọ bn %
7,Cho 100g dd H2SO4 49% tác dụng với 100 g đ NaOH thu đc Na2SO4bn %


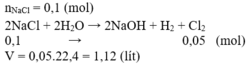
Câu 1 :
mNaCl = 5.85*100/100= 5.85 g
mH2SO4 = 100*49/100=49 g
mNaOH = 100*20/100=20 g
BaSO4 không tan trong nước nên không tính được
Câu 2 :
nNa = 2.3/23 = 0.1 mol
Na + H2O --> NaOH + 1/2H2
0.1___________0.1______0.05
mdd sau phản ứng = 2.3 + 100 - 0.1 = 102.2 g
mNaOH = 4g
C%NaOH = 4/102.2*100% = 3.91%
Câu 3 :
nCa = 0.05 mol
Ca + 2H2O --> Ca(OH)2 + 2H2
0.05____________0.05_____0.1
mdd = 100 + 2 - 0.2 = 101.8 g
mCa(OH)2 = 3.7 g
C%Ca(OH)2 = 3.63%
Câu 4 :
nH2 = 5*10-5 mol
Ca + 2H2O --> Ca(OH)2 + H2
5*10-5__________5*10-5__5*10-5
mCa = 0.002 g
mCa(OH)2 = 0.0037 g
mdd sau phản ứng = 100 g
C%Ca(OH)2 = 0.0037%