Đốt cháy hoàn toàn 6g quặng pirit sắt (FeS2) trong bình chứa khí oxi dư thu được Fe2O3 và SO2.Tính khối lượng Fe2O3 và thể tích của SO2 (đktc)
Help me !!!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{FeS_2}=400.\left(100-10\right)\%=360\left(g\right)\\ \rightarrow n_{FeS_2}=\dfrac{360}{120}=3\left(mol\right)\)
PTHH: 4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
3 3
\(\rightarrow V_{SO_2}=6.22,4=134,4\left(l\right)\)
Fe2O3 oxit bazo, SO2 oxit axit

4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
=> Tổng hệ số chất sản phẩm là: 2+8 = 10

a, PT: \(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\)
\(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
Giả sử: \(\left\{{}\begin{matrix}n_{FeS}=x\left(mol\right)\\n_{FeS_2}=y\left(mol\right)\end{matrix}\right.\)
⇒ 88x + 120y = 17,8 (1)
Ta có: \(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT: \(n_{SO_2}=n_{FeS}+2n_{FeS_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,25 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeS}=0,1.88=8,8\left(g\right)\\m_{FeS_2}=0,075.120=9\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=\dfrac{7}{4}n_{FeS}+\dfrac{11}{4}n_{O_2}=0,38125\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,38125.22,4=8,54\left(l\right)\)
Bạn tham khảo nhé!
a) Gọi nFeS = a (mol)
\(n_{FeS_2}=b\left(mol\right)\) với a; b > 0
\(n_{SO_2}=\dfrac{V}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Ta có: \(\left\{{}\begin{matrix}m_{hh}=17,8=m_{FeS}+m_{FeS_2}=88a+120b\\n_{S\left(SO_2\right)}=0,25=n_{FeS}+2n_{FeS_2}\left(bt\left[S\right]\right)=a+2b\end{matrix}\right.\)
=> a = 0,1(mol); b = 0,075(mol)
mFeS= n.M= 0,1 . 88 = 8,8(g)
=> \(m_{FeS_2}=m_{hh}-m_{FeS}=17,8-8,8=9\left(g\right)\)
b) PT:
\(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\uparrow\\ 4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\uparrow\)
\(Theo2pt\Rightarrow n_{O_2}=\dfrac{7n_{FeS}+11n_{FeS_2}}{4}=0,38125\left(mol\right)\)
\(\Rightarrow V_{O_2}=n\cdot22,4=0,38125\cdot22,4=8,54\left(l\right)\)

Đáp án C
![]()
Vì ![]() nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
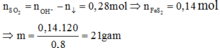

Đáp án C
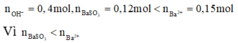
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch

4FeS2 + 11O2 \(\underrightarrow{to}\) 2Fe2O3 + 8SO2
\(n_{FeS_2}=\frac{6}{120}=0,05\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\frac{1}{2}n_{FeS_2}=\frac{1}{2}\times0,05=0,025\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,025\times160=4\left(g\right)\)
Theo pT: \(n_{SO_2}=2n_{FeS_2}=2\times0,05=0,1\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,1\times22,4=2,24\left(l\right)\)
\(n_{FeS_2}=\frac{6}{120}=0,05mol\)
PTHH : \(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
Theo PTHH :
\(n_{SO_2}=\frac{8}{4}n_{FeS_2}=2n_{FeS_2}=2.0,05=0,1mol\) \(\Rightarrow V_{SO_2}=0,1.22,4=2,24l\)
\(n_{Fe_2O_3}=\frac{2}{4}n_{FeS_2}=\frac{1}{2}n_{FeS_2}=\frac{1}{2}.0,05=0,025mol\) \(\Rightarrow m_{Fe_2O_3}=0,025.160=4g\)