trong 1 nhà máy sản xuất rượu, ngta dùng 1 loại nguyên liêu chứa 50% xenlulozo để sản xuất rượu etylic. biết hiệu suất quá trình là 70%. để sản xuất 1 tấn rượu etylic thì khối lượng mùn chưa cần dùng là :
A. 6000kg B. 5031kg C.500kg D.5051kg
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(C6H10O5)n + nH2O -> nC6H12O6
C6H12O6 -men rượu, 30-35 độ C---> 2 C2H5OH + 2 CO2
m(C2H5OH)= 1 (tấn)
=> mC6H12O6(LT)= (1.180)/92=45/23(tấn)
=>mC6H12O6(TT)= 45/23 : 70%=450/161(tấn)
m(xenlulozo LT)= (450/161. 162)/180=405/161(tấn)
=> m(xenlulozo TT)= (450/161): 0,7=4050/1127(tấn)
=> m(mùn cưa)= 4050/1127 : 50%\(\approx\) 7,187(tấn)

Đáp án: D
Ta có sơ đồ: (C6H10O5)n → 2nC2H5OH
Theo phương trình:
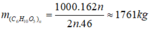
Mà H = 70% → m(C6H10O5)n = 1761 : 70% = 2516 kg → mmùn cưa = 2516 : 50% = 5031 kg
PTHH: (-C6H10O5-)n+nH2\(\underrightarrow{t^o,H_2SO_4}\)nC6H12O6
PTHH: nC6H12O6\(\underrightarrow{enzim}\)2nC2H5OH+2nCO2
Ta có: (-C6H10O5-)n\(\rightarrow\)nC6H12O6\(\rightarrow\)2nC2H5OH
162n 92n (tấn)
x 1 (tấn)
Khối lượng (-C6H10O5-)n cần dùng:
\(m_{\left(-C_6H_{10}O_5-\right)_n}=\dfrac{162.1}{92}:\dfrac{70}{100}\)\(=\dfrac{405}{161}\)(tấn)
K/lượng mùn cưa cần dùng:
\(m_{muncua}=\dfrac{405}{161}:\dfrac{50}{100}=5,031\)(tấn)=5031(kg)
Vậy chọn B.
các bạn trả lời thì ghi cả cách làm ra giúp mình với