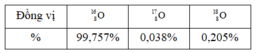
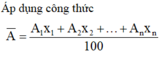Tính nguyên tử khối trung bình của nguyên tố Oxi, biết Oxi có 3 đồng vị : 99,757% 816O; 0,039% 817O; 0,204% 818O .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\overline{M}=\dfrac{99,757.16+0,039.17+0,204.18}{100}=16,004\left(g/mol\right)\)
=> D

\(a.\overline{NTK}_B=\dfrac{10.18,89\%+11.81,11\%}{100\%}=10,8111\left(đ.v.C\right)\\ b.\overline{NTK}_O=\dfrac{16.99,757\%+17.0,039\%+18.0,204\%}{100\%}=16,00447\left(đ.v.C\right)\)

Đáp án C
Áp dụng công thức A ¯ = A 1 x 1 + A 2 x 2 + . . . + A n x n 100 ta có:

\(\overline{M}_O=\dfrac{16.99,76+17.0,039+18.0,201}{100}=16\left(g/mol\right)\)

Khi có 1 nguyên tử 17O, mà % nguyên tử của 17O = 0,039%
⇒ Số nguyên tử O = 1 : 0,039% = 2564 nguyên tử
99,757% 16O ⇒ Số nguyên tử 16O = 99,757%.2564 = 2558 nguyên tử
0,204% 18O ⇒ Số nguyên tử 18O = 0,204%.2564 = 5 nguyên tử

Vì 1 ntử 17O chiếm 0,039% nên lấy 1/0,039% để tính tổng các ntử của các đồng vị khác

HD:
Số nguyên tử của 16O là 99,757/0,039 = 2558 nguyên tử, số nguyên tử 18O là 0,204/0,039 = 5 nguyên tử