B1: R thuộc nhóm VIIA. Trong công thức oxit cao nhất, R chiếm 47,02% về khối lượng
a) Xác định tên nguyên tố R
b) Trong tự nhiên R có 2 đồng vị, đồng vị thứ nhất hơn đồng vị thứ hai là 2 notron, đồng vị thứ nhất chiếm 25%. Xác định số khối của mỗi đồng vị.
B2: Hòa tan 5,6 g hỗn hợp gồm 2 kim loại kiềm liên tiếp nhau vào \(H_2O\) thu được 3,36 lít khí (đktc) và dd A
a) Xác định tên 2 kim loại
b) Tính thể tích dd \(H_2SO_4\) 2M cần dùng để trung hòa hết dd A
Mình đang cần gấp, bạn nào giải giúp mình với !

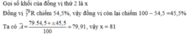
2)
a. Gọi công thức chung (tổng quát) của cả hai kim loại là X.
PTHH: \(X+H_2O\rightarrow XOH+\dfrac{1}{2}H_2\)
1 (mol) .................................. 0.5 (mol)
Theo đề: \(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Theo phương trình có: \(n_X=2n_{H_2}=2.0.15=0.3\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{5.6}{0.3}=18.667\)
Vậy một kim loại phải là Liti (7 đvC) và Na (23 đvC).
b. \(\Rightarrow\)Dung dịch A có 0.3 (mol) XOH. (vì nX = nXOH = 2nH2 ).
PTHH: \(2XOH+H_2SO_4\rightarrow X_2SO_4+2H_2O\)
0.3 (mol) .... 0.15(mol)
Theo phương trình ta được: \(n_{H_2SO_4}=0.15\left(mol\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{0.15}{2}=0.075\left(l\right)\)
1)
a. Vì R thuộc nhóm VIIA nên công thức oxit cao nhất của R có dạng:
R2O7.
R chiếm 47.02% về khối lượng \(\Leftrightarrow\dfrac{2R}{2R+16.7}.100=47.02\Leftrightarrow R=50\left(đvC\right)\)
\(\Rightarrow\) R là thiếc (Sn) nhưng thiếc thuộc chu kì VIA cơ?????????
ĐỀ SAI!!!!!