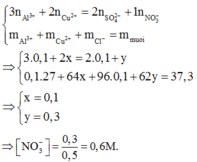Cho 300 ml dung dịch NH3 1M vào 200 ml dung dịch HCI 1M. Tinh CM của các ion NH4+, Cl- và muối NH4Cl trong dung dịch thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


`n_{BaCl_2}=200.10^{-3}.1=0,2(mol)`
`n_{KCl}=100.10^{-3}.2=0,2(mol)`
`->n_{Cl^-}=2n_{BaCl_2}+n_{KCl}=0,6(mol)`
`->[Cl^-]={0,6}/{(200+100).10^{-3}}=2M`

Đáp án A
Áp dụng ĐLBT ĐT: Tổng số mol điện tích dương bằng tổng số mol điện tích âm ta có: 0,1.1+ 0,02.1=0,05.2+ nCl-
Suy ra nCl-= 0,02 mol
Khối lượng chất rắn thu được khi cô cạn dung dịch là:
0,1.18+ 0,02.39+ 96.0,05+ 0,02.35,5= 8,09 gam

Đáp án A
Bảo toàn điện tích : CHCO3 trong 200 ml dung dịch là 2,5M
Xét tổng thể : đổ 300 ml dung dịch A và 200 ml dung dịch
Sau khi trộn :
=> nHCO3 = 2,5.0,2 = 0,5 mol => nCO32- = 0,125 mol
Gọi nồng độ K2CO3 trong A là x => nCO3 tổng = 0,3.(1 + x)
Sau trộn sẽ phản ứng với Ca2+ , Ba2+ => còn lại : 0,3(1 + x) – 0,2 – 0,2 = 0,125
=> x = 0,75M

Đáp án : B
250 ml X phản ứng với 50 ml BaCl2
=> 500 ml X phản ứng với 100 ml BaCl2 => nSO4 = nBa2+ = 0,1 mol
X phản ứng với NH3 => tạo kết tủa Al(OH)3 ( Cu(OH)2 tan trong NH3)
=> nAl3+ = nAl(OH)3 = 0,1 mol
Trong X : Bảo toàn điện tích : 3nAl3+ + 2nCu2+ = nNO3- + 2nSO42-
Laij cos : mmuối X = 27.nAl3+ + 64nCu2+ + 62nNO3 + 96nSO4 = 37,3g
=> nNO3- = 0,3 mol
=> CM(NO3-) = 0,6M